Clinical and pathological characteristics as well as prognosis of adult patients with chronic active Epstein-Barr virus infection
-
摘要:
目的 研究成人慢性活动性EB病毒(EBV)感染患者的临床、病理特点及诊断、治疗方法和预后。 方法 回顾性收集甘肃省某医院2017年1月—2022年12月收治的8例成人慢性活动性EBV感染患者的临床及病理资料,分析其临床及组织病理特点、EBV相关检测结果,以及患者治疗、预后情况。 结果 8例慢性活动性EBV感染患者中,男性3例,女性5例;中位年龄21.5岁,自起病至确诊中位时间为7个月;以发热、血细胞(累及外周血两系或三系)减少、淋巴结及肝脾大为主要表现。血浆EBV核酸(DNA)定量均>1.0×103。EBV感染细胞分选结果显示,3例为T淋巴细胞感染,2例为NK细胞感染,3例为T淋巴细胞和NK细胞共同感染。8例患者骨髓细胞学检查均未见异型淋巴细胞,6例可见噬血细胞。流式细胞术(FCM)分型结果显示,8例患者均未检出异常细胞群,不表达髓细胞、B淋巴细胞、T淋巴细胞及NK细胞标记,T细胞受体(TCR)基因重排阳性率为37.5%(3例),病理组化显示大部分病例(6例,75.0%)表达CD3,部分病例表达CD4、CD8、CD56、TIA-1,EBER均为阳性。患者经治疗后生存率为50.0%(4例),随访时间为6~51个月,1年生存率为85.7%,中位生存时间为24个月。 结论 慢性活动性EBV感染患者临床表现多变,可出现致死性并发症,应尽早诊断,个体化治疗,降低患者病死率。 -
关键词:
- 慢性活动性EB病毒感染 /
- EB病毒 /
- 噬血细胞性淋巴组织细胞增生症
Abstract:Objective To study the clinical and pathological characteristics, as well as diagnosis, treatment methods and prognosis of adult patients with chronic active Epstein-Barr virus infection (CAEBVI). Methods Clinical and pathological data of 8 adult patients with CAEBVI admitted to a hospital in Gansu Province from January 2017 to December 2022 were collected retrospectively, clinical and histopathological characteristics, EBV-related test results, as well as treatment and prognosis of patients were analyzed. Results Among 8 CAEBVI patients, 3 were males and 5 were females, with the median age of 21.5 years. The median time from onset to diagnosis of CAEBVI was 7 months. The main manifestations were fever, pancytopenia (involving two or three peripheral blood lines), as well as lymph node enlargement, hepatomegaly and splenomegaly. The quantifications of plasma EBV nucleic acid (DNA) were all >1.0×103. The sorting results of EBV infected cells showed that 3 cases were T lymphocytes infection, 2 were NK cell infection, and 3 were co-infection of T lymphocytes and NK cells. Bone marrow cytological examination of 8 patients showed no atypical lymphocytes, while 6 patients showed hemophagocytic cells. Flow cytometey (FCM) typing results showed that no abnormal cell population was detected in all the 8 patients, and no myeloid, B lymphocyte, T lymphocyte and NK cell markers were expressed. The positive rate of T cell receptor (TCR) gene rearrangement was 37.5% (n=3). Histopathology showed that most cases (n=6, 75.0%) expressed CD3, partial cases expressed CD4, CD8, CD56, TIA-1, and EBV encoded RNA (EBER), all were positive. The survival rate of patients after treatment was 50.0% (n=4), the follow-up time was 6-51 months, the 1-year survival rate was 85.7%, and the median survival time was 24 months. Conclusion CAEBVI is characterized by variable clinical manifestations that may lead to fatal complications. Early diagnosis and individualized treatment should be performed to reduce mortality of patients. -
EB病毒(Epstein-Barr virus, EBV)是一种人类疱疹双链DNA病毒,属于γ疱疹病毒亚科,正常人群中的感染率在90%以上[1]。当病毒与宿主之间的平衡被破坏时,感染会导致一系列EBV相关的疾病[2],少数EBV感染者病情迁延,并伴有传染性单核细胞增多症(infectious mononucleosis, IM)类似症状反复出现,且有EBV感染引起的组织病理学证据,称为慢性活动性EBV感染(chronic active Epstein-Barr virus infection, CAEBVI)。CAEBVI可以引起多器官功能障碍,极易诱发噬血细胞综合征(hemophagocytic lymphohistiocytosis, HLH)[3], 因临床发病率较低,许多医生对该病的认识不足,导致部分病例不能尽早诊断与治疗,病死率较高。CAEBVI虽在儿童、青少年和成人中均可发病,但目前研究主要针对儿童及青少年群体,而以成人为研究对象的文献较少。本研究回顾性分析了甘肃省人民医院血液科收治的8例CAEBVI成人患者的临床、病理特征、治疗及预后情况,以期提高对该疾病的认识,为CAEBVI的诊治提供经验。
1. 对象与方法
1.1 研究对象
2017年1月—2022年12月甘肃省人民医院收治的8例CAEBVI成人患者,其中男性3例,女性5例;年龄18~54岁,中位年龄21.5岁。所有患者均符合2016版世界卫生组织(WHO)全身性CAEBVI的诊断标准[4]:(1)出现IM症状至少3个月;(2)外周血或病变组织中EBV核酸(DNA)定量升高;(3)外周血或组织病变中的T淋巴细胞或NK细胞发生EBV感染;(4)缺乏可以解释病情的其他疾病的证据。纳入病例中满足以下8条标准中5条或以上的患者可诊断合并HLH。(1)发热:体温>38.5℃,持续7 d;(2)脾大;(3)血细胞减少(累及外周血两系或三系):血红蛋白(Hb)<100 g/L,血小板计数(PLT)<100×109/L,中性粒细胞计数<1.0×109/L,且非骨髓造血功能降低所致;(4)高甘油三酯血症和(或) 低纤维蛋白原血症;(5)在骨髓、脾、肝或淋巴结中发现噬血现象;(6)NK细胞活性降低或缺如;(7)血清铁蛋白升高≥500 μg/L;(8)可溶性白细胞介素-2受体(sCD25)升高。本研究经该院伦理委员会审核批准(2022-421)。
1.2 研究方法
收集患者临床资料,包括性别、年龄、临床表现、EBV特异性抗体、血浆EBV病毒载量、感染EBV的淋巴细胞亚群检测、骨髓形态学、流式细胞学、TCR基因重排、病理组织活检等。
1.3 检测方法
(1) 血浆EBV DNA定量检测及淋巴细胞亚群分选:采用实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction, qPCR)方法。(2)骨髓细胞学检查和流式细胞免疫学检查:骨髓穿刺涂片常规瑞氏染色后观察。(3)骨髓细胞免疫分型:采用四色流式细胞仪,检测抗原包括CD4、CD8、CD3、KAPPA、LAMBDA、CD38、CD20、CD56、CD5、CD10、CD19、CD57、FMC-7、CD200、CD79b、CD23、CD103、CD11c、CD22、CD45。(4)T细胞受体(TCR)基因重排检查:TCRB、TCRD和TCRG基因重排检测均采用PCR方法。(5)组织病理活检和免疫组化检查:免疫组化分析抗原包括CD3、CD4、CD5、CD8、CD10、Bcl-2、Bcl-6、CD23、CD43、CD21、C-MYC、CD30、MUM-1、PAX-5、CD20、CyclinD1、CD56、TIA-1,采用原位杂交方法检测。
1.4 治疗方案
CHOP(环磷酰胺、长春新碱、泼尼松、柔红霉素)、ESCAP(依托泊苷、阿糖胞苷、培门冬酶、甲泼尼龙);合并HLH者给予HLH-1994(地塞米松、依托泊苷、环孢素)、DEP/L-DEP(甲泼尼龙、依托泊苷、脂质体多柔比星±培门冬酶)。
2. 结果
2.1 临床特征
8例CAEBVI患者男女比例为0.6 ∶1,年龄≤25岁者5例,中位年龄21.5岁。自起病至确诊CAEBVI的中位时间为7个月。8例患者中,7例有发热及淋巴结和/或肝脾大,3例有多浆膜腔积液,便血、皮疹各1例,肝功能及凝血功能异常者各5例,合并间质性肺病者3例,合并消化道出血者1例,合并噬血者6例。EBV感染细胞分选结果显示,T淋巴细胞感染3例(病例1、3、4),NK细胞感染2例(病例7、8),T淋巴细胞及NK细胞共同感染3例(病例2、5、6)。见表 1。
表 1 8例CAEBVI患者的临床资料Table 1 Clinical data of 8 CAEBVI patients病例 性别 年龄(岁) 首发症状 发病至确诊时间(个月) 血常规 WBC (×109/L) 淋巴细胞比率(%) Hb (g/L) PLT (×109/L) 1 男性 54 发热、水肿、多浆膜腔积液、血便 4 1.3 65.2 36 70 2 男性 18 发热、淋巴结及脾大 16 0.9 72.3 77 32 3 女性 23 发热,淋巴结、肝、脾大 6 19.3 75.3 101 78 4 女性 27 发热、脾大、多浆膜腔积液 4 1.7 90.6 98 55 5 女性 19 发热、皮疹、淋巴结肿大 5 0.4 57.4 62 11 6 男性 46 发热、淋巴结及肝大 8 2.5 44.8 72 62 7 女性 20 发热、淋巴结及脾大 12 5.9 54.9 108 101 8 女性 18 多浆膜腔积液、淋巴结及脾大 10 9.0 66.9 112 142 病例 凝血指标 生化指标 铁蛋白(ng/mL) IL-2R (U/mL) APTT(s) PT(s) ALT(U/L) AST(U/L) LDH(U/L) BIL(mg/dL) IBIL(mg/dL) 1 38.7 18.8 279 95 414 1.10 2.20 886 >7 500 2 43.0 15.0 34 38 523 0.24 0.82 990 1 535 3 45.3 14.1 713 517 785 2.72 4.51 >2 000 >7 500 4 50.0 15.7 121 233 897 0.86 1.82 622 1 939 5 55.8 15.5 49 82 1 375 0.44 1.52 >2 000 >7 500 6 49.6 16.2 115 46 602 0.54 1.36 788 2 737 7 55.2 18.0 178 67 542 0.37 0.81 422 1 077 8 29.5 14.3 21 44 212 0.25 0.46 323 790 注:WBC为白细胞计数;APTT为活化部分凝血活酶时间(activated partial thromboplastin time);PT为凝血酶原时间(prothrombin time);ALT为丙氨酸转氨酶(alanine transaminase); AST为天冬氨酸转氨酶(aspartate aminotransferase);LDH为乳酸脱氢酶(lactate dehydrogenase);DBIL为直接胆红素(direct bilirubin);IBIL为间接胆红素(indirect bilirubin);IL-2R为白细胞介素2受体(interleukin 2 receptor)。 2.2 骨髓细胞学和流式细胞学检测结果
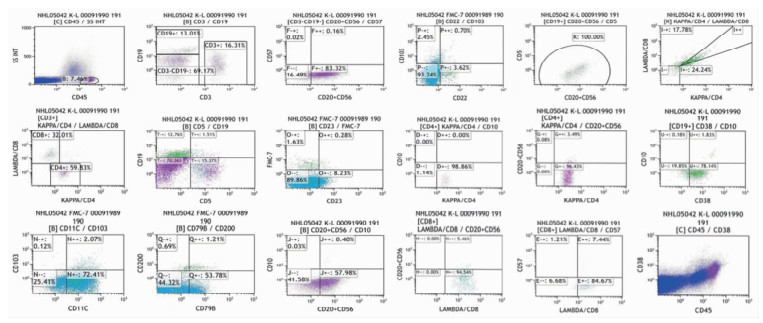
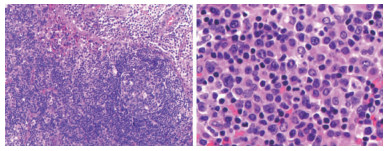
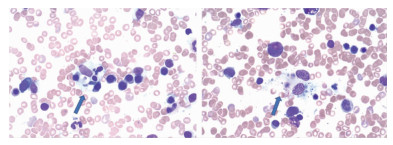
8例患者均进行1次以上骨髓细胞学检查。初次骨髓细胞学检查均显示增生活跃,未发现原始或幼稚细胞,未见异常淋巴细胞;6例患者(病例1~6)表现为噬血现象,巨噬细胞体积较大,胞质丰富呈浅灰色,形态不规则,边缘可见伪足,可见吞噬多个成熟红细胞、幼红细胞、血小板、淋巴细胞等,见图 1。初次骨髓流式细胞术(FCM)检测8例患者均未检出异常细胞群,不表达髓细胞、B淋巴细胞、T淋巴细胞及NK细胞标记,见图 2。
2.3 TCR重排阳性情况
8例CAEBVI患者均进行TCR重排检测,其中3例(病例2、3、8)TCRG重排阳性,余患者TCRB、TCRG、TCRD重排检测均为阴性。
2.4 EBV相关检测结果
8例患者血浆EBV DNA定量均>1.0×103。EBV感染细胞分选结果显示,3例为T淋巴细胞感染,2例为NK细胞感染,3例为T淋巴细胞和NK细胞共同感染。见表 2。
表 2 8例CAEBVI患者EBV相关检测结果Table 2 EBV-related test results of 8 CAEBVI patients病例 血浆EBV DNA定量(cp/mL) 感染EBV淋巴细胞亚群检测及定量(cp/细胞数) EB-VCA-IgM EB-VCA-IgG EA-IgG CD4+ CD8+ CD56+ 1 4.4×105 2.6×106/2×105 / / - + + 2 3.5×105 5.6×105/2×105 / 8.8×104/2×105 + + + 3 2.3×105 4.8×106/2×105 / / - - + 4 2.8×105 2.6×106/2×105 2.6×106/2×105 / - + + 5 3.3×104 / 4.8×105/2×105 8.8×104/2×105 - - + 6 6.0×104 7.4×103/2×105 / 6.2×103/2×105 - - + 7 4.1×103 / / 5.3×104/2×105 - + - 8 7.6×103 / / 2.4×104/2×105 - + + 注:/为未检出;-为检测结果阴性;+为检测结果阳性。 2.5 组织病理活检和免疫组化检查结果
6例患者进行淋巴结活检,主要表现为结构完整或部分结构破坏,增生细胞为淋巴细胞和/或组织细胞;1例患者进行脾穿刺活检,表现为炎性细胞浸润;1例患者进行结肠黏膜组织活检,表现为炎性细胞和淋巴组织浸润,可见中等偏大的淋巴细胞增生。免疫组化结果显示:大部分病例(75.0%,6例)表达CD3,部分病例表达CD4、CD8、CD56、TIA-1,EBV编码核糖核酸(EBV encoded RNA, EBER)均阳性,见图 3。增殖指数Ki-67为40%~90%,见表 3。
表 3 8例CAEBVI患者病理组织学检查结果Table 3 Pathological histopathological examination results of 8 CAEBVI patients病例 免疫组织化学 EBER Ki-67 (%) CD3 CD4 CD8 CD56 TIA-1 1 - / / / ± + 80 2 + + - ± + + 70 3 + + - - + + 70 4 + - ++ - ± + 90 5 + - + + ± + 80 6 + ++ - ± - + 70 7 - - - ± ± + 40 8 ± - - + - + 50 注:/为未检测;-为阴性;+为阳性;±为可疑阳性;+ +为强阳性。 2.6 治疗、转归及预后
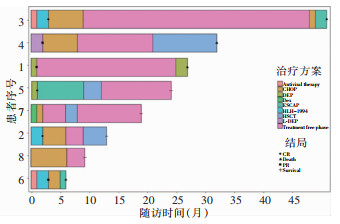
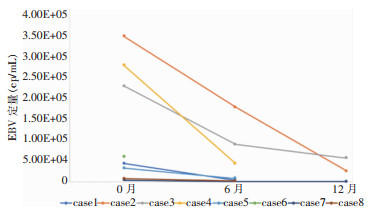
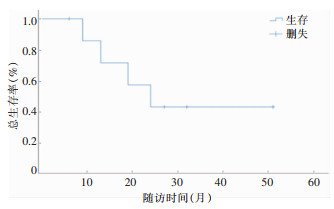
2例患者曾在确诊前接受抗病毒治疗(更昔洛韦), 6例合并HLH患者中,2例给予DEP,1例给予L-DEP,3例给予HLH-1994方案,均达到部分缓解(partial remission, PR)以上治疗反应;6例给予CHOP方案(5例有效,1例无效后给予ESCAP方案),1例患者因合并四肢周围神经病变而给予ESCAP,1例患者经HLH-1994方案治疗HLH缓解后未进行化学治疗;4例(病例2、4、5、7)进行异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation, allo-HSCT), 病例4因移植后出现重度移植物抗宿主病(graft versus host disease, GVHD), 后因血浆EBV DNA转阳、肺部感染死亡;1例患者(病例1)无供者,最终出现心力衰竭,放弃治疗自动出院死亡;1例患者(病例3)因血细胞减少,肝衰竭而死亡;1例患者(病例6)病情进展迅速,治疗后未缓解,最终考虑向侵袭性NK细胞白血病转化可能性大,因肺部感染、血流感染死亡,8例患者具体治疗方案及预后见图 4。在治疗前、治疗后6个月、12个月监测EBV,除病例6病情恶化很快死亡未获得治疗后指标,其他病例治疗后EBV定量较治疗前下降1个数量级(见图 5)。随访6~51个月,所有患者的1年生存率为85.7%,中位生存时间为24个月,95%置信区间为11.1~36.8个月,见图 6。
3. 讨论
EBV初始感染常发生于幼儿期,无明显症状,但发生在青春期时约50%出现IM症状。初始感染后EBV可以在B淋巴细胞内形成潜伏感染,不能彻底清除,且B淋巴细胞不是EBV感染的唯一宿主,上皮细胞、T淋巴细胞和NK细胞也会受到病毒的侵袭,当病毒与宿主之间的平衡被打破后,感染会导致一系列EBV相关的疾病[5]。CAEBVI是EBV感染不同类型细胞(B淋巴细胞、T淋巴细胞、NK细胞) 后引起克隆扩增的一类疾病,西方人中淋巴细胞型CAEBVI相对常见,病死率低,而亚洲人种以T淋巴细胞和NK细胞感染为主,预后差。WHO在2016年将CAEBVI归类于EBV相关T淋巴细胞或NK细胞淋巴增殖性疾病(EBV-T/NK-LPD)[4]。
本研究纳入的8例病例以反复发作的IM症状为表现,包括发热、咽峡炎,肝、脾、淋巴结大和皮疹。还可出现多系统功能障碍,如消化道损伤(腹泻、消化道溃疡、肝功能异常、黄疸)、呼吸系统损伤(以肺间质病变为主)、心血管损伤(心肌炎、血管炎、动脉瘤、肺动脉高压)[6]、神经系统损伤等[7]。CAEBVI还可能导致危及生命的并发症,如HLH[8]、消化道大出血或穿孔、冠脉瘤等[9]。本组患者中有7例(87.5%)以发热为首发症状,给予抗感染或抗病毒治疗,治疗反应性差。后因病情进展,出现多浆膜腔积液、肝功能及凝血功能障碍、消化道出血、呼吸困难等不典型症状,当患者合并HLH,出现血细胞异常时,此时才前往血液专科诊治。
CAEBVI患者的诊断条件中主要以典型的临床表现、外周血或受累组织EBV DNA定量检测升高,且经细胞分选后为T淋巴细胞/NK细胞受感染,并排除免疫缺陷性疾病、恶性肿瘤或自身免疫性疾病所导致的上述临床症状。在诊断条件中要求病程>3个月,但是目前有文献[10]指出不一定局限于时间,而应更重视组织受累情况。EBV相关检查则包括EBV特异性抗体检测、EBV DNA水平测定和活检组织中EBER检测。本研究中8例患者均进行血浆EBV DNA检测,且病毒载量明显高于1.0×103。EB病毒载量可作为CAEBVI病情严重程度及治疗效果的监测指标[11]。8例患者EBV感染细胞分选结果显示,T淋巴细胞感染3例,NK细胞感染2例,T淋巴细胞及NK细胞共同感染3例。T淋巴细胞EBV感染的患者病情进展更为凶险、预后更差[12]。本研究结果显示,4例死亡患者中有3例均为T淋巴细胞感染类型。TCR重排并非CAEBVI诊断或鉴别诊断的条件,但依据文献报道CAEBVI可有TCR多克隆、寡克隆或单克隆重排。因此,在临床中TCR重排检测发现单克隆重排并不能除外CAEBVI,本文纳入的8例患者中,3例TCRG重排阳性。因患者随着病情进展出现血液系统损伤,需要完善骨穿以及免疫分型,当出现淋巴结、肝、脾大或其他脏器受累时往往还会进行组织器官病理活组织检查[13]。本研究结果表明,CAEBVI患者骨髓细胞形态学未出现形态异常的淋巴细胞,合并HLH的患者可见噬血现象。EBV-T/NK-LPD的病理状态包括增生性、交接性和肿瘤性疾病谱系[14],可以分为四类,即类别A1为多形性增生,非肿瘤性,滤泡内CD8+(CD4<CD8,比例倒置),小淋巴细胞聚集;类别A2存在克隆性的EBV感染的细胞,此时细胞处于肿瘤与非肿瘤交界处;类别A3存在克隆性的单核EBV感染的细胞(外周T细胞淋巴瘤或NK细胞淋巴瘤/白血病);类别B会出现暴发性表现,存在克隆性的单核EBV感染的细胞(等同于T细胞淋巴瘤)[15-16]。本研究中,8例患者的病理组织均为A1及A2类,免疫组化显示大部分(75.0%)表达CD3,部分病例表达CD4、CD8、CD56、TIA-1,EBER均阳性,可鉴别于系统性EBV+T细胞淋巴瘤、EBV+NK/T细胞淋巴瘤或急性NK细胞白血病,增殖指数Ki-67为40%~90%。
20世纪90年代后期日本学者提出针对于CAEBVI的“三步疗法”,分别为控制免疫炎症反应、清除EBV感染的淋巴细胞、HSCT实现免疫重建。而传统抗病毒治疗,如阿昔洛韦和更昔洛韦则被认为作用有限,对病毒感染早期可能有效,但当EBV在细胞内复制并扩散至T淋巴细胞/NK细胞时则无效。新型治疗手段方面,靶向治疗和免疫治疗在CAEBVI中的应用取得了一定进展。组蛋白去乙酰化酶(histone deacetylase, HDAC)抑制剂西达本胺可以清除EBV感染的T淋巴细胞;作用于JAK/STAT通路的芦可替尼可以抑制EBV感染的NK细胞或T淋巴细胞增殖以及细胞因子;硼替佐米可以抑制NF-κB通路,抑制NK细胞或T淋巴细胞中TNF-α和IFN-γ mRNA的表达,促进NK细胞或T淋巴细胞凋亡[16-17];程序性死亡受体1(PD-1)及其配体(PD-L1)作用于信号通路,提示免疫检查点亦为治疗CAEBVI的一种创新型策略[18]。而以上治疗中,目前只有HSCT被认为是唯一可能实现治愈的方式,2012年日本学者[19]报道接受HSCT后CAEBVI患者15年的生存率约为60.6%,且患病时间越短移植后无病生存率越高。本研究8例患者中,6例合并HLH患者中,2例给予DEP,1例给予L-DEP,3例给予HLH-1994方案,患者均达到PR以上治疗反应;第二步以清除受感染的淋巴细胞为主要目的,6例患者给予CHOP方案化学治疗,1例患者因合并四肢周围神经病变而给予ESCAP方案,治疗后监测EBV不同程度下降。2例患者(病例1、3)治疗后疾病有数年的缓解期,但最终因再次复发致死;1例患者(病例4)进行allo-HSCT,但移植后EBV病毒定量复升且合并肠道移植物抗宿主病,最终因感染死亡;1例患者(病例6)经过抗噬血、化学治疗后病情短暂缓解,但随后病情迅速进展致死亡。3例患者(病例2、5、7)进行allo-HSCT后目前随访存活。1例患者(病例8)确诊9个月,现积极动员患者进行HSCT治疗。
综上所述,CAEBVI是一种以系统性炎症及肿瘤性增生为双向表现的疾病,异质性较大。本研究中所接诊的患者均表现为侵袭性病程,经规范治疗后病情迅速缓解甚至可稳定数年,但整体预后差,allo-HSCT为可能治愈该病的治疗手段。尽管每例患者年龄、体能评分、合并症、经济因素的差别导致治疗方案的差异性,但临床医生遇到具有该类表现的患者,必须尽快通过其症状、体征及实验室、骨髓检查、病理活检等手段明确诊断,为治疗疗效不佳及症状反复发作的高危患者赢得时间,警惕因合并严重HLH或进展为白血病/淋巴瘤而引起不良结局。
-
表 1 8例CAEBVI患者的临床资料
Table 1 Clinical data of 8 CAEBVI patients
病例 性别 年龄(岁) 首发症状 发病至确诊时间(个月) 血常规 WBC (×109/L) 淋巴细胞比率(%) Hb (g/L) PLT (×109/L) 1 男性 54 发热、水肿、多浆膜腔积液、血便 4 1.3 65.2 36 70 2 男性 18 发热、淋巴结及脾大 16 0.9 72.3 77 32 3 女性 23 发热,淋巴结、肝、脾大 6 19.3 75.3 101 78 4 女性 27 发热、脾大、多浆膜腔积液 4 1.7 90.6 98 55 5 女性 19 发热、皮疹、淋巴结肿大 5 0.4 57.4 62 11 6 男性 46 发热、淋巴结及肝大 8 2.5 44.8 72 62 7 女性 20 发热、淋巴结及脾大 12 5.9 54.9 108 101 8 女性 18 多浆膜腔积液、淋巴结及脾大 10 9.0 66.9 112 142 病例 凝血指标 生化指标 铁蛋白(ng/mL) IL-2R (U/mL) APTT(s) PT(s) ALT(U/L) AST(U/L) LDH(U/L) BIL(mg/dL) IBIL(mg/dL) 1 38.7 18.8 279 95 414 1.10 2.20 886 >7 500 2 43.0 15.0 34 38 523 0.24 0.82 990 1 535 3 45.3 14.1 713 517 785 2.72 4.51 >2 000 >7 500 4 50.0 15.7 121 233 897 0.86 1.82 622 1 939 5 55.8 15.5 49 82 1 375 0.44 1.52 >2 000 >7 500 6 49.6 16.2 115 46 602 0.54 1.36 788 2 737 7 55.2 18.0 178 67 542 0.37 0.81 422 1 077 8 29.5 14.3 21 44 212 0.25 0.46 323 790 注:WBC为白细胞计数;APTT为活化部分凝血活酶时间(activated partial thromboplastin time);PT为凝血酶原时间(prothrombin time);ALT为丙氨酸转氨酶(alanine transaminase); AST为天冬氨酸转氨酶(aspartate aminotransferase);LDH为乳酸脱氢酶(lactate dehydrogenase);DBIL为直接胆红素(direct bilirubin);IBIL为间接胆红素(indirect bilirubin);IL-2R为白细胞介素2受体(interleukin 2 receptor)。 表 2 8例CAEBVI患者EBV相关检测结果
Table 2 EBV-related test results of 8 CAEBVI patients
病例 血浆EBV DNA定量(cp/mL) 感染EBV淋巴细胞亚群检测及定量(cp/细胞数) EB-VCA-IgM EB-VCA-IgG EA-IgG CD4+ CD8+ CD56+ 1 4.4×105 2.6×106/2×105 / / - + + 2 3.5×105 5.6×105/2×105 / 8.8×104/2×105 + + + 3 2.3×105 4.8×106/2×105 / / - - + 4 2.8×105 2.6×106/2×105 2.6×106/2×105 / - + + 5 3.3×104 / 4.8×105/2×105 8.8×104/2×105 - - + 6 6.0×104 7.4×103/2×105 / 6.2×103/2×105 - - + 7 4.1×103 / / 5.3×104/2×105 - + - 8 7.6×103 / / 2.4×104/2×105 - + + 注:/为未检出;-为检测结果阴性;+为检测结果阳性。 表 3 8例CAEBVI患者病理组织学检查结果
Table 3 Pathological histopathological examination results of 8 CAEBVI patients
病例 免疫组织化学 EBER Ki-67 (%) CD3 CD4 CD8 CD56 TIA-1 1 - / / / ± + 80 2 + + - ± + + 70 3 + + - - + + 70 4 + - ++ - ± + 90 5 + - + + ± + 80 6 + ++ - ± - + 70 7 - - - ± ± + 40 8 ± - - + - + 50 注:/为未检测;-为阴性;+为阳性;±为可疑阳性;+ +为强阳性。 -
[1] Cohen JI. Epstein-Barr virus infection[J]. N Engl J Med, 2000, 343(7): 481-492. doi: 10.1056/NEJM200008173430707 [2] Taylor GS, Long HM, Brooks JM, et al. The immunology of Epstein-Barr virus-induced disease[J]. Annu Rev Immunol, 2015, 33: 787-821. doi: 10.1146/annurev-immunol-032414-112326 [3] 中国医师协会血液科医师分会, 中华医学会儿科学分会血液学组, 噬血细胞综合征中国专家联盟. 中国噬血细胞综合征诊断与治疗指南(2022年版)[J]. 中华医学杂志, 2022, 102(20): 1492-1499. doi: 10.3760/cma.j.cn112137-20220310-00488 Hematology Branch of Chinese Medical Doctor Association, Hematology Group of Chinese Medical Association Pediatrics Branch, Chinese Expert Alliance of Hemophagocytic syndrome. Chinese Guidelines for diagnosis and treatment of hemophagocytic syndrome (2022 edition)[J]. National Medical Journal of China, 2022, 102(20): 1492-1499. doi: 10.3760/cma.j.cn112137-20220310-00488 [4] Swerdlow SH, Campo E, Pileri SA, et al. The 2016 revision of the World Health Organization classification of lymphoid neo- plasms[J]. Blood, 2016, 127(20): 2375-2390. doi: 10.1182/blood-2016-01-643569 [5] Kawamoto K, Miyoshi H, Suzuki T, et al. A distinct subtype of Epstein-Barr virus-positive T/NK-cell lymphoproliferative disorder: adult patients with chronic active Epstein-Barr virus infection-like features[J]. Haematologica, 2018, 103(6): 1018-1028. doi: 10.3324/haematol.2017.174177 [6] 徐娜, 范洪伟, 黄晓明, 等. 成人慢性活动性EB病毒感染的临床特征分析[J]. 中华内科杂志, 2018, 57(11): 811-815. doi: 10.3760/cma.j.issn.0578-1426.2018.11.004 Xu N, Fan HW, Huang XM, et al. Clinical features of adult patients with chronic active Epstein-Barr virus infection[J]. Chinese Journal of Internal Medicine, 2018, 57(11): 811-815. doi: 10.3760/cma.j.issn.0578-1426.2018.11.004 [7] 肖逸, 张凌云, 曾朝阳, 等. 成人EB病毒性肺炎合并EB病毒性脑炎一例报告[J]. 中国感染控制杂志, 2022, 21(7): 686-689. Xiao Y, Zhang LY, Zeng ZY, et al. EB virus pneumonia complicated with EB virus encephalitis in an adult: a case report[J]. Chinese Journal of Infection Control, 2022, 21(7): 686-689. [8] 吴飞凤, 佘周, 罗森林, 等. 儿童感染相关噬血细胞综合征继发急性早幼粒细胞白血病一例并文献复习[J]. 中国感染控制杂志, 2022, 21(3): 268-272. Wu FF, She Z, Luo SL, et al. Acute promyelocytic leukemia secondary to infection-associated hemophagocytic lymphohistio- cytosis in children: a case report and literature review[J]. Chinese Journal of Infection Control, 2022, 21(3): 268-272. [9] 杨小舟, 杨清銮, 陈宇明, 等. 成人EB病毒感染相关性疾病的临床特征及预后分析[J]. 中华传染病杂志, 2021, 39(3): 163-167. Yang XZ, Yang QL, Chen YM, et al. Analysis of clinical characteristics and prognosis of Epstein-Barr virus-related di-seases in adults[J]. Chinese Journal of Infectious Diseases, 2021, 39(3): 163-167. [10] 杨小舟, 郑建铭, 李荣宽, 等. 慢性活动性EB病毒感染相关性肠炎三例[J]. 中华传染病杂志, 2020, 38(6): 371-373. doi: 10.3760/cma.j.cn311365-20190814-00262 Yang XZ, Zheng JM, Li RK, et al. Three cases of chronic active enteritis associated with Epstein-Barr virus infection[J]. Chinese Journal of Infectious Diseases, 2020, 38(6): 371-373. doi: 10.3760/cma.j.cn311365-20190814-00262 [11] Okano M, Kawa K, Kimura H, et al. Proposed guidelines for diagnosing chronic active Epstein-Barr virus infection[J]. Am J Hematol, 2005, 80(1): 64-69. doi: 10.1002/ajh.20398 [12] 郑晓丹, 周小鸽, 金妍, 等. 成年人系统性EB病毒阳性T/NK细胞淋巴组织增殖性疾病的临床病理研究[J]. 中华病理学杂志, 2011, 40(4): 227-234. Zheng XD, Zhou XG, Jin Y, et al. Clinicopathologic features of systemic EBV-positive T/NK-cell lymphoproliferative di-sease in adults[J]. Chinese Journal of Pathology, 2011, 40(4): 227-234. [13] Fujiwara S, Nakamura H. Chronic active Epstein-Barr virus infection: is it immunodeficiency, malignancy, or both?[J]. Cancers (Basel), 2020, 12(11): 3202. doi: 10.3390/cancers12113202 [14] 陈文, 宋国新, 王震. 消化道慢性活动性EB病毒感染3例临床病理学分析[J]. 中华病理学杂志, 2022, 51(10): 1019-1023. Chen W, Song GX, Wang Z. Chronic active Epstein-Barr virus infection in the gastrointestinal tract: a clinicopathological study of three cases[J]. Chinese Journal of Pathology, 2022, 51(10): 1019-1023. [15] 周小鸽, 张燕林, 谢建兰, 等. 对EB病毒相关淋巴组织增殖性疾病的理解和认识[J]. 中华病理学杂志, 2016, 45(12): 817-821. Zhou XG, Zhang YL, Xie JL, et al. The understanding of Epstein-Barr virus associated lymphoproliferative disorder[J]. Chinese Journal of Pathology, 2016, 45(12): 817-821. [16] 明茜, 肖毅. 异基因造血干细胞移植治疗慢性活动性EB病毒感染的研究进展[J]. 临床内科杂志, 2020, 37(7): 523-525. Ming X, Xiao Y. Research progress of allogeneic hematopoie-tic stem cell transplantation in the treatment of chronic active Epstein-Barr virus infection[J]. Journal of Clinical Internal Medicine, 2020, 37(7): 523-525. [17] 周哲, 邵凌云, 张文宏. 慢性活动性EB病毒感染临床诊断与治疗进展[J]. 临床血液学杂志, 2022, 35(1): 11-15. Zhou Z, Shao LY, Zhang WH. Progress in clinical diagnosis and treatment of chronic active Epstein-Barr virus infection[J]. Journal of Clinical Hematology, 2022, 35(1): 11-15. [18] 吴佳颖, 徐斌, 朱晓健, 等. PD-1抑制剂治疗慢性活动性EB病毒感染6例报告并文献复习[J]. 中华血液学杂志, 2023, 44(2): 165-168. Wu JY, Xu B, Zhu XJ, et al. PD-1 inhibitor in chronic active Epstein-Barr virus infection: a report of six cases and literature review[J]. Chinese Journal of Hematology, 2023, 44(2): 165-168. [19] Bollard CM, Cohen JI. How I treat T-cell chronic active Epstein-Barr virus disease[J]. Blood, 2018, 131(26): 2899-2905.

 下载:
下载: