Antimicrobial resistance of bacteria from cerebrospinal fluid specimens: surveillance report from Hunan Province Antimicrobial Resistance Survei-llance System, 2012-2021
-
摘要:
目的 了解湖南省脑脊液标本分离细菌的分布及耐药性变迁, 为临床正确诊断及合理用药提供参考。 方法 收集湖南省细菌耐药监测网2012—2021年各成员单位上报数据, 参照全国细菌耐药监测网(CARSS)技术方案执行, 应用WHONET 5.6和SPSS 20.0软件对脑脊液标本分离细菌及其药敏结果数据进行分析。 结果 2012—2021年湖南省细菌耐药监测网成员单位脑脊液标本共分离细菌11 837株, 前5位依次为凝固酶阴性葡萄球菌(6 397株, 54.0%)、鲍曼不动杆菌(764株, 6.5%)、金黄色葡萄球菌(606株, 5.1%)、屎肠球菌(465株, 3.9%)、大肠埃希菌(447株, 3.8%); 耐甲氧西林凝固酶阴性葡萄球菌(MRCNS)的检出率为58.9%~66.3%, 耐甲氧西林金黄色葡萄球菌(MRSA)的检出率为34.4%~62.1%, 未发现对万古霉素、利奈唑胺和替考拉宁耐药的葡萄球菌属细菌; 屎肠球菌检出率高于粪肠球菌, 屎肠球菌对青霉素、氨苄西林、高浓度链霉素、左氧氟沙星的耐药率高于粪肠球菌(均P=0.001);肺炎链球菌对青霉素的耐药率为85.0%, 处于较高水平; 大肠埃希菌对头孢曲松的耐药率>60%, 对含酶抑制剂和碳青霉烯类抗生素的耐药率较低; 肺炎克雷伯菌对头孢曲松的耐药率>60%, 对含酶抑制剂哌拉西林/他唑巴坦、头孢哌酮/舒巴坦的耐药率>30%, 对碳青霉烯类药物(亚胺培南、美罗培南)耐药率在30%左右; 鲍曼不动杆菌对大部分测试药物的耐药率>60%, 对亚胺培南和美罗培南的耐药率为59.0%~79.4%, 对多黏菌素B保持较低水平耐药。 结论 脑脊液标本分离细菌中, 凝固酶阴性葡萄球菌占比最高, 病原菌整体耐药情况较为严重, 细菌耐药监测对中枢神经系统感染的有效治疗非常重要。 Abstract:Objective To investigate changes in the distribution and antimicrobial resistance of bacteria isolated from cerebrospinal fluid (CSF) specimens in Hunan Province, and provide reference for correct clinical diagnosis and rational antimicrobial use. Methods Data reported by member units of Hunan Province Antimicrobial Resistance Surveillance System from 2012 to 2021 were collected according to China Antimicrobial Resistance Surveillance System (CARSS) technical scheme. Data of bacteria isolated from CSF specimens and antimicrobial susceptibility testing results were analyzed with WHONET 5.6 and SPSS 20.0 software. Results A total of 11 837 bacterial strains were isolated from CSF specimens from member units of Hunan Province Antimicrobial Resistance Surveillance System from 2012 to 2021. The top 5 strains were coagulase-negative Staphylococcus (n=6 397, 54.0%), Acinetobacter baumannii (n=764, 6.5%), Staphylococcus aureus (n=606, 5.1%), Enterococcus faecium (n=465, 3.9%), and Escherichia coli (n=447, 3.8%). The detection rates of methicillin-resistant coagulase-negative Staphyloco-ccus (MRCNS) and methicillin-resistant Staphylococcus aureus (MRSA) were 58.9%-66.3% and 34.4%-62.1%, respectively. No Staphylococcus spp. were found to be resistant to vancomycin, linezolid, and teicoplanin. The detection rate of Enterococcus faecium was higher than that of Enterococcus faecalis, and the resistance rates of Enterococcus faecium to penicillin, ampicillin, high concentration streptomycin and levofloxacin were all higher than those of Enterococcus faecalis (all P=0.001). Resistance rate of Streptococcus pneumoniae to penicillin was 85.0%, at a high level. Resistance rate of Escherichia coli to ceftriaxone was >60%, while resistance rates to enzyme inhibitors and carbapenem antibiotics were low. Resistance rate of Klebsiella pneumoniae to ceftriaxone was >60%, to enzyme inhibitors piperacillin/tazobactam and cefoperazone/sulbactam was >30%, to carbapenem imipenem and me-ropenem was about 30%. Resistance rates of Acinetobacter baumannii to most tested antimicrobial agents were > 60%, to imipenem and meropenem were 59.0%-79.4%, to polymyxin B was low. Conclusion Among the bacteria isolated from CSF specimens, coagulase-negative Staphylococcus accounts for the largest proportion, and the overall resistance of pathogenic bacteria is relatively serious. Bacterial antimicrobial resistance surveillance is very important for the effective treatment of central nerve system infection. -
中枢神经系统感染是临床上最为严重的感染之一, 具有发病急、治疗时间长、难以治愈等诸多特点,需选用敏感且能通过血脑屏障的药物进行早期、联合治疗。
细菌性脑膜炎是临床上最常见和严重的中枢神经系统感染性疾病,早期、正确的抽取脑脊液标本进行细菌学检查可为临床提供重要的病原学诊断依据和治疗指导[1],对改善患者预后尤为重要。为掌握湖南省脑脊液标本分离菌的分布及耐药变迁,为制定和评价抗菌药物临床应用管理政策提供有效的科学依据,现将2012—2021年湖南省脑脊液标本分离细菌的监测结果汇总报告如下。
1. 资料与方法
1.1 数据来源
全部监测数据来自2012—2021年湖南省细菌耐药监测网各成员单位。各监测网点医院将细菌监测数据从医院信息系统、药敏测定系统录入WHONET 5.6软件,通过湖南省细菌耐药监测网上报,要求上报细菌药敏的最低抑菌浓度(minimum inhibitory concentration, MIC)或抑菌圈直径大小。
1.2 技术方案
细菌鉴定方法、质控菌株选择及测试抗菌药物种类按照全国细菌耐药监测网(CARSS)技术方案执行[2-6]。药敏试验结果依据美国临床实验室标准化协会(Clinical & Laboratory Standards Institute, CLSI)推荐的抗微生物药敏试验执行标准2022年版(M100第32版)进行判断[7],结果分为敏感(S)、中介/剂量依赖型敏感(I/SDD)、耐药(R)三种情况,因受篇幅限制,结果中未将I/SDD列出。其中头孢哌酮/舒巴坦无药敏解释折点,参照头孢哌酮折点判断[8-9]。替加环素采用美国食品药品监督管理局(Food and Drug Administration, FDA)推荐的折点[10]。多黏菌素B参考欧盟药敏试验标准委员会(European Committee on Antimicrobial Susceptibility Testing, EUCAST)推荐折点[11]。
1.3 统计分析
依据每例患者相同标本统计第一株细菌的原则,剔除重复菌株,采用WHONET 5.6软件进行药敏结果分析。应用SPSS 20.0软件进行数据统计分析,采用趋势卡方检验推断耐药率的变迁趋势。检验水准α=0.05。
2. 结果
2.1 2012—2021年脑脊液分离菌株构成
2.1.1 菌株构成
2012—2021年湖南省细菌耐药监测网成员单位脑脊液标本分离细菌以革兰阳性菌为主,占比为65.03%~77.70%,革兰阴性菌占比为22.30%~34.97%,见图 1。
2.1.2 菌株分布
2012—2021年湖南省细菌耐药监测网成员单位脑脊液标本共分离细菌11 837株,占比为0.4%~0.7%,前5位依次为凝固酶阴性葡萄球菌(CNS, 54.0%)、鲍曼不动杆菌(6.5%)、金黄色葡萄球菌(5.1%)、屎肠球菌(3.9%)及大肠埃希菌(3.8%),菌种分布见表 1。
表 1 2012—2021年湖南省细菌耐药监测网脑脊液标本分离细菌的菌种分布Table 1 Distribution of bacterial species isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021细菌 2012—2013年 2014—2015年 2016—2017年 2018—2019年 2020—2021年 合计 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) CNS 441 43.8 1 042 50.6 1 549 52.5 1 778 57.2 1 587 58.5 6 397 54.0 鲍曼不动杆菌 78 7.7 161 7.8 212 7.2 179 5.7 134 4.9 764 6.5 金黄色葡萄球菌 91 9.0 135 6.6 147 5.0 123 3.9 110 4.0 606 5.1 屎肠球菌 27 2.7 83 4.0 117 4.0 127 4.1 111 4.1 465 3.9 大肠埃希菌 52 5.1 99 4.8 121 4.1 105 3.4 70 2.6 447 3.8 肺炎克雷伯菌 33 3.3 56 2.7 89 3.0 100 3.2 91 3.4 369 3.1 肺炎链球菌 36 3.6 45 2.2 57 1.9 62 2.0 49 1.8 249 2.1 粪肠球菌 29 2.9 55 2.7 65 2.2 52 1.7 34 1.3 235 2.0 铜绿假单胞菌 13 1.3 44 2.1 47 1.6 37 1.2 37 1.4 178 1.5 阴沟肠杆菌 12 1.2 22 1.1 28 0.9 16 0.5 22 0.8 100 0.9 其他细菌 195 19.4 317 15.4 516 17.6 531 17.1 468 17.2 2 027 17.1 合计 1 007 100 2 059 100 2 948 100 3 110 100 2 713 100 11 837 100 2.2 2012—2021年脑脊液标本分离菌对抗菌药物的耐药性变迁
2.2.1 葡萄球菌属
在分离的CNS中,前5位细菌为表皮葡萄球菌(38.9%)、溶血葡萄球菌(19.7%)、人葡萄球菌(12.9%)、头状葡萄球菌(9.6%)、沃氏葡萄球菌(4.6%)。耐甲氧西林凝固酶阴性葡萄球菌(MRCNS)的检出率为58.9%~66.3%,耐甲氧西林金黄色葡萄球菌(MRSA)的检出率为34.4%~62.1%,未发现对万古霉素、利奈唑胺和替考拉宁耐药的葡萄球菌属细菌。CNS对庆大霉素、克林霉素、复方磺胺甲
 表 2 2012—2021年湖南省细菌耐药监测网脑脊液标本分离CNS对常见抗菌药物的药敏试验结果Table 2 Antimicrobial susceptibility testing results of coagulase-negative Staphylococcus isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
表 2 2012—2021年湖南省细菌耐药监测网脑脊液标本分离CNS对常见抗菌药物的药敏试验结果Table 2 Antimicrobial susceptibility testing results of coagulase-negative Staphylococcus isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021抗菌药物 2012—2013年 2014—2015年 2016—2017年 2018—2019年 2020—2021年 r P 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 青霉素 406 87.2 12.8 1 005 83.8 16.2 1 503 87.3 12.7 1 688 87.8 12.2 1 510 89.0 11.0 0.007 0.423 苯唑西林 409 63.3 36.7 1 007 59.4 40.6 1 523 61.5 38.5 1 697 62.2 37.8 1 537 64.8 35.2 0.010 0.315 庆大霉素 403 21.6 68.7 1 025 21.2 68.5 1 542 20.7 71.5 1 762 18.0 75.5 1 578 16.5 76.2 -0.036 0.002 万古霉素 415 0 100 1 009 0 100 1 535 0 100 1 756 0 100 1 568 0 100 / / 替考拉宁 88 0 100 222 0 100 281 0 100 501 0 100 605 0 100 / / 利奈唑胺 353 0 100 900 0 100 1 498 0 100 1 724 0 100 1 554 0 100 / / 红霉素 417 67.6 24.9 997 69.9 23.7 1 465 69.5 28.2 1 646 70.4 27.8 1 495 65.6 32.6 -0.007 0.506 克林霉素 409 32.8 63.6 989 34.6 60.3 1 461 27.3 69.9 1 621 24.2 73.4 1 472 22.0 74.9 -0.064 0.001 左氧氟沙星 339 34.5 54.9 845 41.2 53.8 1 352 39.9 57.5 1 521 36.5 61.2 1 460 39.9 57.7 0.001 0.926 复方磺胺甲 
358 40.5 58.9 927 40.1 59.8 1 487 36.7 63.3 1 721 29.5 70.5 1 499 25.8 74.2 -0.071 0.001 利福平 392 13.3 82.7 1 007 10.4 86.7 1 541 10.9 88.3 1 757 9.4 89.7 1 546 9.0 90.8 -0.028 0.019 注:/表示无统计分析;仅对耐药率进行趋势检验。 表 3 2012—2021年湖南省细菌耐药监测网脑脊液标本分离金黄色葡萄球菌和CNS对常见抗菌药物的药敏试验结果Table 3 Antimicrobial susceptibility testing results of Staphylococcus aureus and coagulase-negative Staphylococcus isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021抗菌药物 金黄色葡萄球菌 CNS χ2 P 检测株数 R(%) S(%) 检测株数 R(%) S(%) 青霉素 587 92.8 7.2 6 101 87.3 12.7 0.976 0.323 苯唑西林 588 45.6 54.4 6 162 62.3 37.7 16.795 0.001 庆大霉素 602 20.1 75.7 6 299 18.9 73.3 0.342 0.559 万古霉素 596 0 100 6 272 0 100 / / 替考拉宁 210 0 100 1 696 0 100 / / 利奈唑胺 575 0 100 6 018 0 100 / / 红霉素 549 64.1 31.0 6 009 68.7 28.2 0.939 0.332 克林霉素 570 32.5 63.5 5 492 26.7 70.1 4.774 0.029 左氧氟沙星 504 27.2 69.0 5 507 38.8 57.9 12.873 0.001 复方磺胺甲 
568 18.7 81.3 5 981 32.6 67.4 26.817 0.001 利福平 601 11.0 85.9 6 232 10.0 88.8 0.476 0.490 注:上表为2012—2021年葡萄球菌数据合并分析,/表示未进行卡方检验;仅对耐药率进行分析。 2.2.2 肠球菌属
屎肠球菌检出率高于粪肠球菌,屎肠球菌对青霉素、氨苄西林、高浓度链霉素、左氧氟沙星的耐药率高于粪肠球菌(均P=0.001),而两者对高浓度庆大霉素、万古霉素、替考拉宁、利奈唑胺、利福平的耐药率没有明显差异。屎肠球菌检出4株对万古霉素耐药的菌株,粪肠球菌未检出对万古霉素、替考拉宁的耐药株。见表 4。
表 4 2012—2021年湖南省细菌耐药监测网脑脊液标本分离肠球菌属对常见抗菌药物的药敏试验结果Table 4 Antimicrobial susceptibility testing results of Enterococcus spp. isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021抗菌药物 屎肠球菌 粪肠球菌 χ2 P 检测株数 R(%) S(%) 检测株数 R(%) S(%) 青霉素 438 88.1 11.9 209 8.1 91.9 113.896 0.001 氨苄西林 427 88.3 11.7 212 6.1 93.9 126.253 0.001 高浓度庆大霉素 250 36.8 63.2 134 23.9 75.4 3.520 0.061 高浓度链霉素 187 49.2 50.8 79 17.7 82.3 10.994 0.001 万古霉素 459 0.9 98.7 222 0 99.1 1.929 0.165 替考拉宁 114 0.9 99.1 59 0 100 0.516 0.473 利奈唑胺 432 0.5 98.8 214 1.4 95.8 1.612 0.204 左氧氟沙星 402 75.6 15.2 192 20.8 75.0 50.119 0.001 利福平 77 77.9 10.4 44 65.9 22.7 0.323 0.570 注:上表为2012—2021年肠球菌数据合并分析;仅对耐药率进行分析。 2.2.3 肺炎链球菌
在脑脊液标本中肺炎链球菌分离率低,大部分年份分离株数都小于30,10年数据合并作药敏分析,肺炎链球菌对青霉素的耐药率为85.0%,处于较高水平,对于头孢曲松、美罗培南的耐药率分别为16.8%、15.6%,对万古霉素、左氧氟沙星保持低水平耐药,耐药率分别为0.9%、4.6%。见表 5。
表 5 2012—2021年湖南省细菌耐药监测网脑脊液标本分离肺炎链球菌对常见抗菌药物药敏试验结果Table 5 Antimicrobial susceptibility testing results of Streptococcus pneumoniae isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021抗菌药物 检测株数 R(%) S(%) 青霉素 214 85.0 15.0 阿莫西林/克拉维酸 47 6.4 78.7 头孢呋辛 50 68.0 30.0 头孢曲松 208 16.8 60.1 头孢噻肟 79 26.6 40.5 美罗培南 199 15.6 60.3 万古霉素 235 0.9 99.1 左氧氟沙星 217 4.6 93.5 注:上表为2012—2021年肺炎链球菌数据合并分析。 2.2.4 大肠埃希菌及肺炎克雷伯菌
2012—2021年脑脊液标本分离的大肠埃希菌对氨苄西林耐药率均>70%,对第三代头孢类抗生素头孢曲松耐药率>60%,对喹诺酮类的左氧氟沙星、环丙沙星耐药率均>50%,对阿米卡星保持较低耐药率(1.2%),对含酶抑制剂哌拉西林/他唑巴坦的耐药率为7.9%。肺炎克雷伯菌对氨苄西林天然耐药,对头孢曲松耐药率>60%,对含酶抑制剂哌拉西林/他唑巴坦、头孢哌酮/舒巴坦的耐药率分别为36.9%、36.3%, 对碳青霉烯类抗生素,如亚胺培南、美罗培南,其耐药率在30%左右。对比两种菌的耐药情况,肺炎克雷伯菌对哌拉西林/他唑巴坦、头孢他啶、头孢吡肟、头孢哌酮/舒巴坦、头孢西丁、亚胺培南、美罗培南、阿米卡星、妥布霉素的耐药率均高于大肠埃希菌(均P < 0.05)。而对环丙沙星、复方磺胺甲
 表 6 2012—2021年湖南省细菌耐药监测网脑脊液标本分离大肠埃希菌和肺炎克雷伯菌对常见抗菌药物的药敏试验结果Table 6 Antimicrobial susceptibility testing results of Escherichia coli and Klebsiella pneumoniae isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
表 6 2012—2021年湖南省细菌耐药监测网脑脊液标本分离大肠埃希菌和肺炎克雷伯菌对常见抗菌药物的药敏试验结果Table 6 Antimicrobial susceptibility testing results of Escherichia coli and Klebsiella pneumoniae isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021抗菌药物 大肠埃希菌 肺炎克雷伯菌 χ2 P 检测株数 R(%) S(%) 检测株数 R(%) S(%) 氨苄西林 325 82.5 15.4 - - - / / 氨苄西林/舒巴坦 258 43.8 31.4 222 58.6 34.2 3.392 0.066 哌拉西林/他唑巴坦 406 7.9 70.0 355 36.9 49.0 61.218 0.001 头孢唑林 294 68.0 12.2 265 70.6 14.0 0.077 0.782 头孢呋辛 203 54.2 36.0 188 65.4 30.9 1.294 0.255 头孢他啶 387 32.3 60.7 311 50.2 45.7 9.647 0.002 头孢曲松 361 60.9 38.5 306 63.7 36.3 0.127 0.722 头孢噻肟 38 28.9 63.2 # # # / / 头孢吡肟 426 31.5 53.1 359 48.2 45.4 9.961 0.002 头孢哌酮/舒巴坦 192 8.9 85.4 179 36.3 57.0 26.004 0.001 头孢西丁 230 15.2 80.0 190 42.6 55.8 21.986 0.001 氨曲南 334 42.8 51.8 298 52.3 43.3 2.049 0.152 亚胺培南 361 8.9 88.9 288 28.5 68.8 29.474 0.001 美罗培南 209 14.8 84.2 191 31.9 66.5 10.306 0.001 阿米卡星 429 1.2 98.6 360 20.8 77.8 67.283 0.001 庆大霉素 383 36.6 58.2 316 37.7 61.1 0.042 0.838 妥布霉素 265 14.3 56.2 229 26.6 59.0 7.686 0.006 左氧氟沙星 396 55.3 21.2 340 42.9 38.5 3.799 0.051 环丙沙星 328 63.4 27.1 265 35.5 54.3 15.321 0.001 复方磺胺甲 
411 56.2 43.8 354 39.5 60.5 7.412 0.006 注:上表为2012—2021年大肠埃希菌、肺炎克雷伯菌数据合并分析;-表示天然耐药;#表示分析菌株数小于30;/表示未进行卡方检验;仅对耐药率进行分析。 2.2.5 鲍曼不动杆菌
2012—2021年脑脊液标本分离的鲍曼不动杆菌对大部分测试药物的耐药率>60%;对米诺环素较敏感,耐药率<30%;对多黏菌素B保持较低水平耐药(耐药率为0~2.8%);对亚胺培南和美罗培南的耐药率为59.0%~79.4%。采用Cochrane-Armitage线性趋势检验,仅对头孢哌酮/舒巴坦耐药率的变化有统计学意义(P < 0.05),有逐年增高的趋势(r=0.136),对其他药物的耐药率变化均无统计学意义(均P>0.05)。见表 7。
表 7 2012—2021年湖南省细菌耐药监测网脑脊液标本分离鲍曼不动杆菌对常见抗菌药物药敏试验结果Table 7 Antimicrobial susceptibility testing results of Acinetobacter baumannii isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021抗菌药物 2012—2013年 2014—2015年 2016—2017年 2018—2019年 2020—2021年 r P 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 氨苄西林/舒巴坦 43 62.8 32.6 110 68.2 26.4 99 72.7 26.3 92 69.6 25.0 72 61.1 33.3 -0.006 0.879 哌拉西林/他唑巴坦 64 64.1 28.1 151 63.6 25.8 157 61.1 34.4 128 70.3 26.6 116 65.5 29.3 0.011 0.723 头孢他啶 61 77.0 16.4 117 67.5 26.5 161 67.1 29.2 138 76.1 23.2 119 68.9 30.2 -0.001 0.982 头孢吡肟 58 72.4 22.4 159 73.6 26.4 211 65.4 34.1 178 71.3 23.6 132 62.9 31.1 -0.018 0.517 头孢哌酮/舒巴坦 # # # 65 15.4 56.9 73 30.1 53.4 116 44.8 31.0 111 45.9 41.4 0.136 0.002 亚胺培南 56 71.4 25.0 149 71.1 26.8 174 63.8 34.5 147 76.9 22.4 110 67.3 31.8 0.001 0.976 美罗培南 # # # 53 73.6 15.1 100 59.0 40.0 102 79.4 20.6 97 67.0 31.9 0.007 0.866 阿米卡星 35 42.9 42.9 82 53.7 45.1 135 52.6 46.7 93 50.5 46.2 82 40.2 56.1 -0.024 0.547 庆大霉素 61 62.3 27.9 160 68.8 27.5 206 66.0 31.1 150 68.0 28.7 92 52.2 42.4 -0.021 0.483 妥布霉素 50 56.0 36.0 121 55.4 38.0 147 69.4 29.3 118 61.0 34.7 100 56.0 42.0 0.003 0.938 米诺环素 # # # # # # 44 6.8 77.3 57 22.8 57.9 81 17.3 64.2 0.072 0.294 左氧氟沙星 57 47.4 31.6 147 52.4 36.1 190 47.9 36.3 154 55.2 28.6 118 50.8 37.3 0.009 0.767 环丙沙星 60 66.7 23.3 156 67.3 31.4 175 69.7 29.7 139 71.9 27.3 105 67.6 31.4 0.006 0.841 多黏菌素B # # # # # # 36 2.8 94.4 37 0 100 40 0 100 -0.118 0.213 注:#表示分析菌株数小于30;仅对耐药率进行趋势检验。 2.3 重要耐药菌变迁情况
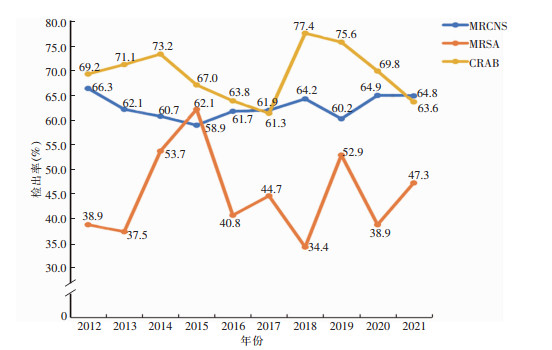
2012—2021年MRCNS检出率在58.9%~66.3%间波动,未见明显趋势,除2015年外均高于MRSA;耐碳青霉烯类鲍曼不动杆菌(CRAB)检出率>60%,相对稳定;其它重要耐药菌由于每年检测株数较少,未做分析。2012—2021年脑脊液标本分离的重要耐药菌检出率变化趋势见图 2。
3. 讨论
2012—2021年湖南省细菌耐药监测网脑脊液标本共分离细菌11 837株,占比为0.4%~0.7%,与CARSS 2014—2019年脑脊液标本细菌耐药监测报告[12]数据相近(0.5%~0.8%)。
脑脊液标本分离细菌中,CNS居首位,检出率从2012—2013年的43.8%上升至2020—2021年的58.5%,呈现逐年上升趋势,远高于第二位分离细菌。在分离的CNS中,以表皮葡萄球菌(38.9%)、溶血葡萄球菌(19.7%)最多,与国外文献[13]一致。我国临床脑脊液感染患者以神经外科手术后感染为主,神经科CNS检出率明显高于非神经科室[14]。CNS是皮肤和黏膜的定植菌,易黏附于导管/假体的表面并形成生物膜,是导管/假体相关感染的主要致病因素[12]。当患者存在免疫力低下、颅脑手术等危险因素时极易引发感染,CNS通过产生黏液和表达黏液相关抗原而产生毒力,并可产生致病性的厚生物膜[15]。当脑脊液中分离到CNS, 首先要排除标本污染的可能性,综合其它检查结果,如脑脊液常规、生化等检查,并结合患者的临床症状来判断是否有感染的可能,找出真正的病原体,提高病原学诊断水平。
鲍曼不动杆菌占比居脑脊液标本分离菌中第二位(6.5%),2012—2021年检出率为4.9%~7.8%;对大部分测试药物的耐药率>60%,对米诺环素较敏感(耐药率<30%),对多黏菌素B保持较低水平耐药(耐药率为0~2.8%);仅对头孢哌酮/舒巴坦的耐药率有逐年增高趋势,变化有统计学意义(r=0.136,P < 0.05)。鲍曼不动杆菌能形成生物膜,其多重耐药性加上血脑屏障对抗菌药物的作用,限制了抗菌药物在临床的治疗范围[14]。专家共识推荐根据药敏情况选择2种药物联合(头孢哌酮/舒巴坦或氨苄西林/舒巴坦+替加环素或多西环素;舒巴坦+碳青霉烯类;替加环素+头孢哌酮/舒巴坦、氨苄西林/舒巴坦、碳青霉烯类、多黏菌素;多黏菌素+碳青霉烯类或替加环素) 或3种药物联合(头孢哌酮/舒巴坦+替加环素+碳青霉烯类;头孢哌酮/舒巴坦+多西环素+碳青霉烯类;亚胺培南+利福平+多黏菌素或妥布霉素)[16],以达到更好的治疗效果。
金黄色葡萄球菌占比居脑脊液标本分离菌第三位(5.1%),2012—2021年MRSA检出率为34.4%~62.1%,与CARSS 2014—2019年脑脊液标本细菌耐药监测报告[12]结果相当。未发现对万古霉素、利奈唑胺和替考拉宁耐药的葡萄球菌属细菌。比较金黄色葡萄球菌和CNS的药敏情况,金黄色葡萄球菌对克林霉素的耐药率高于CNS(P < 0.05),但对苯唑西林、左氧氟沙星和复方磺胺甲
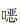
屎肠球菌占比居脑脊液标本分离菌第四位(3.9%),其检出率高于粪肠球菌,对青霉素、氨苄西林、高浓度链霉素、左氧氟沙星的耐药率高于粪肠球菌(均P=0.001)。对于高度耐药的阳性菌脑脊液感染重症患者,容易透过血脑屏障的万古霉素和利奈唑胺应为治疗首选,而替考拉宁无法透过血脑屏障[17],因此,在治疗阳性菌引起的中枢神经系统感染时应充分、综合考虑药物敏感性、血脑屏障穿透性和患者身体情况等因素[14]。
肠杆菌目分离菌中,大肠埃希菌占比居脑脊液标本分离菌第五位(3.8%),肺炎克雷伯菌为第六位(3.1%),阴沟肠杆菌为第十位(0.9%)。大肠埃希菌对第三代头孢菌素耐药率较高,对含酶抑制剂类和碳青霉烯类抗生素耐药性低。值得注意的是,肺炎克雷伯菌对碳青霉烯类药物如亚胺培南、美罗培南耐药率在30%左右。治疗产超广谱β-内酰胺酶的肺炎克雷伯菌与大肠埃希菌时,若对碳青霉烯类抗生素敏感则推荐使用美罗培南而非亚胺培南,美罗培南在非炎性或轻度炎性、严重脑膜炎患者的脑脊液透过率分别为4.7%~25%、39%[18],而亚胺培南因可降低癫痫发作的阈值,应避免使用[19-20]。碳青霉烯类耐药菌多为泛耐药菌,同时对多种抗菌药物耐药。因此,对碳青霉烯类耐药菌进行筛查和防控对于控制医院感染尤为重要[12]。
2012—2021年脑脊液标本分离的肺炎链球菌、铜绿假单胞菌、阴沟肠杆菌株数较少,其中肺炎链球菌对青霉素的耐药率为85.0%,对万古霉素、左氧氟沙星保持低水平耐药,耐药率分别为0.9%、4.6%,铜绿假单胞菌对大多数常用抗菌药物耐药率均<30%,阴沟肠杆菌对氨苄西林、阿莫西林/克拉维酸、氨苄西林/舒巴坦、头孢唑林、头孢西丁天然耐药,临床用药时应注意。
中枢神经系统感染是临床上最为严重的感染之一,取脑脊液标本进行细菌学检验可为临床提供重要的疾病诊断依据和精准的抗感染治疗,显著改善患者预后,正确采集并及时处理脑脊液标本十分重要。脑脊液培养应尽可能排除因污染菌存在而导致的假阳性,并及时有效地与临床沟通。抗感染治疗时选择抗菌药物除考虑病原菌敏感的抗菌药物外,也应考虑易透过血脑屏障的抗菌药物,如头孢曲松、头孢噻肟、美罗培南及万古霉素等,进入脑脊液可以维持有效的药物浓度,以便获得更好的临床疗效。
-
表 1 2012—2021年湖南省细菌耐药监测网脑脊液标本分离细菌的菌种分布
Table 1 Distribution of bacterial species isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
细菌 2012—2013年 2014—2015年 2016—2017年 2018—2019年 2020—2021年 合计 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) 株数 构成比(%) CNS 441 43.8 1 042 50.6 1 549 52.5 1 778 57.2 1 587 58.5 6 397 54.0 鲍曼不动杆菌 78 7.7 161 7.8 212 7.2 179 5.7 134 4.9 764 6.5 金黄色葡萄球菌 91 9.0 135 6.6 147 5.0 123 3.9 110 4.0 606 5.1 屎肠球菌 27 2.7 83 4.0 117 4.0 127 4.1 111 4.1 465 3.9 大肠埃希菌 52 5.1 99 4.8 121 4.1 105 3.4 70 2.6 447 3.8 肺炎克雷伯菌 33 3.3 56 2.7 89 3.0 100 3.2 91 3.4 369 3.1 肺炎链球菌 36 3.6 45 2.2 57 1.9 62 2.0 49 1.8 249 2.1 粪肠球菌 29 2.9 55 2.7 65 2.2 52 1.7 34 1.3 235 2.0 铜绿假单胞菌 13 1.3 44 2.1 47 1.6 37 1.2 37 1.4 178 1.5 阴沟肠杆菌 12 1.2 22 1.1 28 0.9 16 0.5 22 0.8 100 0.9 其他细菌 195 19.4 317 15.4 516 17.6 531 17.1 468 17.2 2 027 17.1 合计 1 007 100 2 059 100 2 948 100 3 110 100 2 713 100 11 837 100 表 2 2012—2021年湖南省细菌耐药监测网脑脊液标本分离CNS对常见抗菌药物的药敏试验结果
Table 2 Antimicrobial susceptibility testing results of coagulase-negative Staphylococcus isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
抗菌药物 2012—2013年 2014—2015年 2016—2017年 2018—2019年 2020—2021年 r P 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 青霉素 406 87.2 12.8 1 005 83.8 16.2 1 503 87.3 12.7 1 688 87.8 12.2 1 510 89.0 11.0 0.007 0.423 苯唑西林 409 63.3 36.7 1 007 59.4 40.6 1 523 61.5 38.5 1 697 62.2 37.8 1 537 64.8 35.2 0.010 0.315 庆大霉素 403 21.6 68.7 1 025 21.2 68.5 1 542 20.7 71.5 1 762 18.0 75.5 1 578 16.5 76.2 -0.036 0.002 万古霉素 415 0 100 1 009 0 100 1 535 0 100 1 756 0 100 1 568 0 100 / / 替考拉宁 88 0 100 222 0 100 281 0 100 501 0 100 605 0 100 / / 利奈唑胺 353 0 100 900 0 100 1 498 0 100 1 724 0 100 1 554 0 100 / / 红霉素 417 67.6 24.9 997 69.9 23.7 1 465 69.5 28.2 1 646 70.4 27.8 1 495 65.6 32.6 -0.007 0.506 克林霉素 409 32.8 63.6 989 34.6 60.3 1 461 27.3 69.9 1 621 24.2 73.4 1 472 22.0 74.9 -0.064 0.001 左氧氟沙星 339 34.5 54.9 845 41.2 53.8 1 352 39.9 57.5 1 521 36.5 61.2 1 460 39.9 57.7 0.001 0.926 复方磺胺甲 
358 40.5 58.9 927 40.1 59.8 1 487 36.7 63.3 1 721 29.5 70.5 1 499 25.8 74.2 -0.071 0.001 利福平 392 13.3 82.7 1 007 10.4 86.7 1 541 10.9 88.3 1 757 9.4 89.7 1 546 9.0 90.8 -0.028 0.019 注:/表示无统计分析;仅对耐药率进行趋势检验。 表 3 2012—2021年湖南省细菌耐药监测网脑脊液标本分离金黄色葡萄球菌和CNS对常见抗菌药物的药敏试验结果
Table 3 Antimicrobial susceptibility testing results of Staphylococcus aureus and coagulase-negative Staphylococcus isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
抗菌药物 金黄色葡萄球菌 CNS χ2 P 检测株数 R(%) S(%) 检测株数 R(%) S(%) 青霉素 587 92.8 7.2 6 101 87.3 12.7 0.976 0.323 苯唑西林 588 45.6 54.4 6 162 62.3 37.7 16.795 0.001 庆大霉素 602 20.1 75.7 6 299 18.9 73.3 0.342 0.559 万古霉素 596 0 100 6 272 0 100 / / 替考拉宁 210 0 100 1 696 0 100 / / 利奈唑胺 575 0 100 6 018 0 100 / / 红霉素 549 64.1 31.0 6 009 68.7 28.2 0.939 0.332 克林霉素 570 32.5 63.5 5 492 26.7 70.1 4.774 0.029 左氧氟沙星 504 27.2 69.0 5 507 38.8 57.9 12.873 0.001 复方磺胺甲 
568 18.7 81.3 5 981 32.6 67.4 26.817 0.001 利福平 601 11.0 85.9 6 232 10.0 88.8 0.476 0.490 注:上表为2012—2021年葡萄球菌数据合并分析,/表示未进行卡方检验;仅对耐药率进行分析。 表 4 2012—2021年湖南省细菌耐药监测网脑脊液标本分离肠球菌属对常见抗菌药物的药敏试验结果
Table 4 Antimicrobial susceptibility testing results of Enterococcus spp. isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
抗菌药物 屎肠球菌 粪肠球菌 χ2 P 检测株数 R(%) S(%) 检测株数 R(%) S(%) 青霉素 438 88.1 11.9 209 8.1 91.9 113.896 0.001 氨苄西林 427 88.3 11.7 212 6.1 93.9 126.253 0.001 高浓度庆大霉素 250 36.8 63.2 134 23.9 75.4 3.520 0.061 高浓度链霉素 187 49.2 50.8 79 17.7 82.3 10.994 0.001 万古霉素 459 0.9 98.7 222 0 99.1 1.929 0.165 替考拉宁 114 0.9 99.1 59 0 100 0.516 0.473 利奈唑胺 432 0.5 98.8 214 1.4 95.8 1.612 0.204 左氧氟沙星 402 75.6 15.2 192 20.8 75.0 50.119 0.001 利福平 77 77.9 10.4 44 65.9 22.7 0.323 0.570 注:上表为2012—2021年肠球菌数据合并分析;仅对耐药率进行分析。 表 5 2012—2021年湖南省细菌耐药监测网脑脊液标本分离肺炎链球菌对常见抗菌药物药敏试验结果
Table 5 Antimicrobial susceptibility testing results of Streptococcus pneumoniae isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
抗菌药物 检测株数 R(%) S(%) 青霉素 214 85.0 15.0 阿莫西林/克拉维酸 47 6.4 78.7 头孢呋辛 50 68.0 30.0 头孢曲松 208 16.8 60.1 头孢噻肟 79 26.6 40.5 美罗培南 199 15.6 60.3 万古霉素 235 0.9 99.1 左氧氟沙星 217 4.6 93.5 注:上表为2012—2021年肺炎链球菌数据合并分析。 表 6 2012—2021年湖南省细菌耐药监测网脑脊液标本分离大肠埃希菌和肺炎克雷伯菌对常见抗菌药物的药敏试验结果
Table 6 Antimicrobial susceptibility testing results of Escherichia coli and Klebsiella pneumoniae isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
抗菌药物 大肠埃希菌 肺炎克雷伯菌 χ2 P 检测株数 R(%) S(%) 检测株数 R(%) S(%) 氨苄西林 325 82.5 15.4 - - - / / 氨苄西林/舒巴坦 258 43.8 31.4 222 58.6 34.2 3.392 0.066 哌拉西林/他唑巴坦 406 7.9 70.0 355 36.9 49.0 61.218 0.001 头孢唑林 294 68.0 12.2 265 70.6 14.0 0.077 0.782 头孢呋辛 203 54.2 36.0 188 65.4 30.9 1.294 0.255 头孢他啶 387 32.3 60.7 311 50.2 45.7 9.647 0.002 头孢曲松 361 60.9 38.5 306 63.7 36.3 0.127 0.722 头孢噻肟 38 28.9 63.2 # # # / / 头孢吡肟 426 31.5 53.1 359 48.2 45.4 9.961 0.002 头孢哌酮/舒巴坦 192 8.9 85.4 179 36.3 57.0 26.004 0.001 头孢西丁 230 15.2 80.0 190 42.6 55.8 21.986 0.001 氨曲南 334 42.8 51.8 298 52.3 43.3 2.049 0.152 亚胺培南 361 8.9 88.9 288 28.5 68.8 29.474 0.001 美罗培南 209 14.8 84.2 191 31.9 66.5 10.306 0.001 阿米卡星 429 1.2 98.6 360 20.8 77.8 67.283 0.001 庆大霉素 383 36.6 58.2 316 37.7 61.1 0.042 0.838 妥布霉素 265 14.3 56.2 229 26.6 59.0 7.686 0.006 左氧氟沙星 396 55.3 21.2 340 42.9 38.5 3.799 0.051 环丙沙星 328 63.4 27.1 265 35.5 54.3 15.321 0.001 复方磺胺甲 
411 56.2 43.8 354 39.5 60.5 7.412 0.006 注:上表为2012—2021年大肠埃希菌、肺炎克雷伯菌数据合并分析;-表示天然耐药;#表示分析菌株数小于30;/表示未进行卡方检验;仅对耐药率进行分析。 表 7 2012—2021年湖南省细菌耐药监测网脑脊液标本分离鲍曼不动杆菌对常见抗菌药物药敏试验结果
Table 7 Antimicrobial susceptibility testing results of Acinetobacter baumannii isolated from CSF specimens, Hunan Province Antimicrobial Resistance Surveillance System, 2012-2021
抗菌药物 2012—2013年 2014—2015年 2016—2017年 2018—2019年 2020—2021年 r P 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 检测株数 R (%) S (%) 氨苄西林/舒巴坦 43 62.8 32.6 110 68.2 26.4 99 72.7 26.3 92 69.6 25.0 72 61.1 33.3 -0.006 0.879 哌拉西林/他唑巴坦 64 64.1 28.1 151 63.6 25.8 157 61.1 34.4 128 70.3 26.6 116 65.5 29.3 0.011 0.723 头孢他啶 61 77.0 16.4 117 67.5 26.5 161 67.1 29.2 138 76.1 23.2 119 68.9 30.2 -0.001 0.982 头孢吡肟 58 72.4 22.4 159 73.6 26.4 211 65.4 34.1 178 71.3 23.6 132 62.9 31.1 -0.018 0.517 头孢哌酮/舒巴坦 # # # 65 15.4 56.9 73 30.1 53.4 116 44.8 31.0 111 45.9 41.4 0.136 0.002 亚胺培南 56 71.4 25.0 149 71.1 26.8 174 63.8 34.5 147 76.9 22.4 110 67.3 31.8 0.001 0.976 美罗培南 # # # 53 73.6 15.1 100 59.0 40.0 102 79.4 20.6 97 67.0 31.9 0.007 0.866 阿米卡星 35 42.9 42.9 82 53.7 45.1 135 52.6 46.7 93 50.5 46.2 82 40.2 56.1 -0.024 0.547 庆大霉素 61 62.3 27.9 160 68.8 27.5 206 66.0 31.1 150 68.0 28.7 92 52.2 42.4 -0.021 0.483 妥布霉素 50 56.0 36.0 121 55.4 38.0 147 69.4 29.3 118 61.0 34.7 100 56.0 42.0 0.003 0.938 米诺环素 # # # # # # 44 6.8 77.3 57 22.8 57.9 81 17.3 64.2 0.072 0.294 左氧氟沙星 57 47.4 31.6 147 52.4 36.1 190 47.9 36.3 154 55.2 28.6 118 50.8 37.3 0.009 0.767 环丙沙星 60 66.7 23.3 156 67.3 31.4 175 69.7 29.7 139 71.9 27.3 105 67.6 31.4 0.006 0.841 多黏菌素B # # # # # # 36 2.8 94.4 37 0 100 40 0 100 -0.118 0.213 注:#表示分析菌株数小于30;仅对耐药率进行趋势检验。 -
[1] 刘运德, 楼永良, 王辉, 等. 临床微生物学检验技术[M]. 北京: 人民卫生出版社, 2015: 383. Liu YD, Lou YL, Wang H, et al. Clinical microbiology laboratory technology[M]. Beijing: People's Medical Publishing House, 2015: 383. [2] 全国细菌耐药监测网. 《全国细菌耐药监测网技术方案(2022年版)》修订说明[EB/OL]. (2022-04-06)[2022-11-15]. https://www.carss.cn/Notice/Details/823. China Antimicrobial Resistance Surveillance System. Revision explanation of The technical plan for the China Antimicrobial Resistance Surveillance System (2022 Edition)[EB/OL]. (2022-04-06)[2022-11-15]. https://www.carss.cn/Notice/Details/823. [3] 全国细菌耐药监测网. 关于印发《全国细菌耐药监测网技术方案(2014版)》的通知: 卫合药委[2014]19号[EB/OL]. (2014-08-25)[2022-11-15]. https://www.carss.cn/Notice/Details/199. China Antimicrobial Resistance Surveillance System. Notice on issuing The technical plan for the China Antimicrobial Resis-tance Surveillance System (2014 Edition): Health and Drug Commission[2014] No. 19[EB/OL]. (2014-08-25)[2022-11-15]. https://www.carss.cn/Notice/Details/199. [4] 全国细菌耐药监测网. 关于印发《全国细菌耐药监测网技术方案(2016版)》的通知: 国卫合药委〔2016〕2号[EB/OL]. (2016-08-09)[2022-11-15]. https://www.carss.cn/Notice/Details/332. China Antimicrobial Resistance Surveillance System. Notice on issuing The technical plan for the China Antimicrobial Resis-tance Surveillance System (2016 Edition): National Health and Drug Commission[2016] No. 2[EB/OL]. (2016-08-09)[2022-11-15]. https://www.carss.cn/Notice/Details/332. [5] 全国细菌耐药监测网. 关于印发《全国细菌耐药监测网技术方案(2018版)》的通知: 国卫合药委〔2018〕1号[EB/OL]. (2018-03-21)[2022-11-15]. https://www.carss.cn/Notice/Details/416. China Antimicrobial Resistance Surveillance System. Notice on issuing The technical plan for the China Antimicrobial Resis-tance Surveillance System (2018 Edition): National Health and Drug Commission[2018] No. 1[EB/OL]. (2018-03-21)[2022-11-15]. https://www.carss.cn/Notice/Details/416. [6] 全国细菌耐药监测网. 关于印发《全国细菌耐药监测网技术方案(2020年版)》和《全国细菌耐药监测网网点医院微生物实验室质量和能力要求(2020年版)》的通知: 国卫合药委〔2020〕1号[EB/OL]. (2020-01-03)[2022-11-15]. https://www.carss.cn/Notice/Details/654. China Antimicrobial Resistance Surveillance System. Notice on issuing The Technical Plan for the China Antimicrobial Resis-tance Surveillance System (2020 Edition) and The quality and capability requirements for microbial laboratories in hospitals of the China Antimicrobial Resistance Surveillance System (2020 Edition): National Health and Drug Commission[2020] No. 1[EB/OL]. (2020-01-03)[2022-11-15]. https://www.carss.cn/Notice/Details/654. [7] CLSI. Performance standards for antimicrobial susceptibility testing: M100, 32nd edition[S]. Malvern, PA, USA: CLSI, 2022. [8] Barry AL, Jones RN. Criteria for disk susceptibility tests and quality control guidelines for the cefoperazone-sulbactam combination[J]. J Clin Microbiol, 1988, 26(1): 13-17. doi: 10.1128/jcm.26.1.13-17.1988 [9] Jones RN, Barry AL, Packer RR, et al. In vitro antimicrobial spectrum, occurrence of synergy, and recommendations for dilution susceptibility testing concentrations of the cefoperazone-sulbactam combination[J]. J Clin Microbiol, 1987, 25(9): 1725-1729. doi: 10.1128/jcm.25.9.1725-1729.1987 [10] U.S. Food & Drug Administration. Tigecycline-injection products[EB/OL]. (2023-01-26)[2023-08-04]. https://www.fda.gov/drugs/development-resources/tigecycline-injection-products. [11] Satlin MJ, Lewis JS, Weinstein MP, et al. Clinical and laboratory standards institute and European committee on antimicrobial susceptibility testing position statements on polymyxin B and colistin clinical breakpoints[J]. Clin Infect Dis, 2020, 71(9): e523-e529. [12] 全国细菌耐药监测网. 全国细菌耐药监测网2014—2019年脑脊液标本细菌耐药监测报告[J]. 中国感染控制杂志, 2021, 20(1): 43-51. http://www.zggrkz.com/zggrkzzz/article/abstract/2024-4-415?st=search China Antimicrobial Resistance Surveillance System. Antimicrobial resistance of bacteria from cerebrospinal fluid specimens: surveillance report from China Antimicrobial Resistance Surveillance System in 2014-2019[J]. Chinese Journal of Infection Control, 2021, 20(1): 43-51. http://www.zggrkz.com/zggrkzzz/article/abstract/2024-4-415?st=search [13] Becker K, Heilmann C, Peters G. Coagulase-negative Staphy-lococci[J]. Clin Microbiol Rev, 2014, 27(4): 870-926. doi: 10.1128/CMR.00109-13 [14] 张树永, 王晓明, 刘家云, 等. 2018—2020年多中心脑脊液分离菌分布及耐药性分析[J]. 中国抗生素杂志, 2021, 46(11): 994-1001. doi: 10.3969/j.issn.1001-8689.2021.11.002 Zhang SY, Wang XM, Liu JY, et al. Distribution and drug resistance of multicenter cerebrospinal fluid isolates from 2018 to 2020[J]. Chinese Journal of Antibiotics, 2021, 46(11): 994-1001. doi: 10.3969/j.issn.1001-8689.2021.11.002 [15] Chang CJ, Ye JJ, Yang CC, et al. Influence of third-generation cephalosporin resistance on adult in-hospital mortality from post-neurosurgical bacterial meningitis[J]. J Microbiol Immunol Infect, 2010, 43(4): 301-309. doi: 10.1016/S1684-1182(10)60047-3 [16] 王明贵. 广泛耐药革兰阴性菌感染的实验诊断、抗菌治疗及医院感染控制: 中国专家共识[J]. 中国感染与化疗杂志, 2017, 17(1): 82-93. https://www.cnki.com.cn/Article/CJFDTOTAL-KGHL201701015.htm Wang MG. Laboratory diagnosis, clinical management and infection control of the infections caused by extensively drug-resistant Gram-negative bacilli: a Chinese consensus statement[J]. Chinese Journal of Infection and Chemotherapy, 2017, 17(1): 82-93. https://www.cnki.com.cn/Article/CJFDTOTAL-KGHL201701015.htm [17] 中国医师协会神经外科医师分会神经重症专家委员会, 北京医学会神经外科学分会神经外科危重症学组. 神经外科中枢神经系统感染诊治中国专家共识(2021版)[J]. 中华神经外科杂志, 2021, 37(1): 2-15. Neurology Intensive Care Expert Committee of the Neurosurgery Branch of the Chinese Medical Association, Neurosurgery Critical Care Group of Neurosurgery Branch of Beijing Medical Association. Chinese expert consensus on the diagnosis and treatment of neurosurgical central nervous system infections(2021 Edition)[J]. Chinese Journal of Neurosurgery, 2021, 37(1): 2-15. [18] Nau R, Sörgel F, Eiffert H. Penetration of drugs through the blood-cerebrospinal fluid/blood-brain barrier for treatment of central nervous system infections[J]. Clin Microbiol Rev, 2010, 23(4): 858-883. doi: 10.1128/CMR.00007-10 [19] van de Beek D, Brouwer MC, Thwaites GE, et al. Advances in treatment of bacterial meningitis[J]. Lancet, 2012, 380(9854): 1693-1702. doi: 10.1016/S0140-6736(12)61186-6 [20] 中国医药教育协会感染疾病专业委员会, 中华结核和呼吸杂志编辑委员会, 中国药学会药物临床评价研究专业委员会. 抗菌药物超说明书用法专家共识[J]. 中华结核和呼吸杂志, 2015, 38(6): 410-444. https://www.cnki.com.cn/Article/CJFDTOTAL-YAXU201902003.htm Infectious Disease Professional Committee of China Medical Education Association, Editorial Committee of Chinese Journal of Tuberculosis and Respiratory Diseases, Clinical Evaluation and Research Committee of Chinese Pharmaceutical Association. Expert consensus on the excessive use of antimicrobial agents beyond the instruction[J]. Chinese Journal of Tuberculosis and Respiratory Diseases, 2015, 38(6): 410-444. https://www.cnki.com.cn/Article/CJFDTOTAL-YAXU201902003.htm

 下载:
下载: