2. 上海交通大学医学院附属仁济医院, 上海 200127;
3. 江苏省人民医院感染管理处, 江苏 南京 210029;
4. 西安交通大学医学部公共卫生学院流行病与卫生统计学系, 陕西 西安 710048;
5. 上海市儿童医院 上海交通大学医学院附属儿童医院感控办, 上海 200062;
6. 江苏省疾病预防控制中心, 江苏 南京 210009;
7. 浙江省疾病预防控制中心, 浙江 杭州 310057;
8. 中南大学湘雅医院医院感染控制中心, 湖南 长沙 410008;
9. 北京大学第一医院感染管理-疾病预防控制处, 北京 100034;
10. 四川大学华西医院医院感染管理部, 四川 成都 610041;
11. 解放军总医院第一医学中心疾病预防控制科, 北京 100853;
12. 杭州市疾病预防控制中心消媒所, 浙江 杭州 310021;
13. 中国疾病预防控制中心环境与健康相关产品安全所, 北京 100021;
14. 上海市卫生健康委员会监督所, 上海 200031;
15. 甘肃省第二人民医院, 甘肃 兰州 730099;
16. 上海市疾病预防控制中心消毒与感染控制科, 上海 200336;
17. 上海市第一人民医院医院感染与疾病预防控制办公室, 上海 201620;
18. 复旦大学附属中山医院感染病科, 上海 200032
2. Renji Hospital, Shanghai Jiao Tong University School of Medicine, Shanghai 200127, China;
3. Department of Infection Management, Jiangsu Province Hospital, Nanjing 210029, China;
4. Department of Epidemiology and Health Statistics, School of Public Health, Xi'an Jiaotong University Health Science Center, Xi'an 710048, China;
5. Department of Infection Control, Shanghai Children's Hospital, School of Medicine, Shanghai Jiao Tong University, Shanghai 200062, China;
6. Jiangsu Provincial Center for Disease Control and Prevention, Nanjing 210009, China;
7. Zhejiang Provincial Center for Disease Control and Prevention, Hangzhou 310057, China;
8. Center for Healthcare associated Infection Control, Xiangya Hospital, Central South University, Changsha 410008, China;
9. Department of Infection Management-Disease Control and Prevention, Peking University First Hospital, Beijing 100034, China;
10. Department of Healthcare-associated Infection Management, West China Hospital, Sichuan University, Chengdu 610041, China;
11. Department of Disease Prevention and Control, the First Medical Center, Chinese PLA General Hospital, Beijing 100853, China;
12. Department of Disinfection and Vector Control, Hangzhou Center for Disease Control and Prevention, Hangzhou 310021, China;
13. National Institute for Environmental Health, Chinese Center for Disease Control and Prevention, Beijing 100021, China;
14. Supervision Institute of Shanghai Municipal Health Commission, Shanghai 200031, China;
15. Second Provincial People's Hospital of Gansu, Lanzhou 730099, China;
16. Department of Disinfection and Infection Control, Shanghai Municipal Center for Disease Control and Prevention, Shanghai 200336, China;
17. Office of Healthcare-associated Infection and Disease Prevention and Control, Shanghai General Hospital, Shanghai 201620, China;
18. Department of Infectious Diseases, Zhong-shan Hospital, Fudan University, Shanghai 200032, China
2020年以来,新型冠状病毒(简称新冠病毒)感染肆虐全球,也不断变异,截至2021年12月下旬,美国新冠病毒新发感染大多为奥密克戎变异株导致。奥密克戎的刺突蛋白有超过30种突变,包括已在其他值得关注的变异株(VOC)中发现的突变,这些突变增加了病毒的传染性[1]。新冠病毒在不锈钢、聚氯乙烯(PVC)面屏、丁腈手套、Tyvek合成材料、医用防护口罩和N100口罩等表面4~7 d后失去活性,而在棉布等多孔、干燥材料上,新冠病毒存活时间明显缩短,棉和加强丁腈手套表面的新冠病毒分别在1、4 h即失去活性。不同个人防护用品(PPE)材料上的新冠病毒在5~7 d内具有传染性[2]。一项通过通风管感染动物的研究,证实了奥密克戎变异株通过气溶胶传播的可能[3]。气溶胶的浓度、接触的距离和时间都会影响传播风险。2023年1月8日起,新冠病毒正式被列为“乙类乙管”,几乎所有医疗机构均面临收治新冠病毒感染者的可能性,为避免环境空气及物体表面污染造成的新冠病毒传播,医疗机构应加强终末消毒。
近期相关研究发现,多种消毒剂(包括浓度为62%~71%的乙醇) 能在短时间内灭活一些与新冠病毒有亲缘关系的冠状病毒。试验条件下,模拟日光可以在15~20 min内灭活新冠病毒,且紫外线C段(ultraviolet C, UVC)水平越高,灭活速度越快[4-5]。
1 基本要求 1.1 适用范围所有收治新冠病毒感染者的医疗机构终末消毒。
1.2 消毒原则空气首选开窗通风[6],可选用过氧化氢气化等方法消毒,负压隔离病房的空气不需要进行终末消毒[7];环境物体表面及仪器设备首选擦拭消毒,不建议采用喷洒消毒,尤其不应采用消毒剂对人体直接喷洒消毒。
1.3 消毒产品所用消毒产品应符合国家有关规定和标准、规范的管理要求,合规、有效。国家卫生健康委员会依法监管的新消毒产品以外的消毒剂、消毒器械应按照《消毒产品卫生安全评价技术要求》 WS 628—2018进行卫生安全评价,合格者方可使用。
1.4 个人防护实施消毒操作的工作人员应戴帽子、医用防护口罩、手套、防水隔离衣。
1.5 第三方消毒服务及消毒效果检测评价机构资质第三方消毒服务机构应具有相应资质,具备专业消毒服务的能力,使用的消毒产品合规有效,并能保证消毒服务质量。消毒效果检测评价机构应通过实验室资质认证。
2 终末消毒方案 2.1 消毒范围和消毒原则收治新冠病毒感染者的医疗机构就诊患者的床单元及周围环境。重点消毒患者床单元,其他区域按《医疗机构环境表面清洁与消毒管理规范》WS/T 512—2016进行常规清洁消毒。
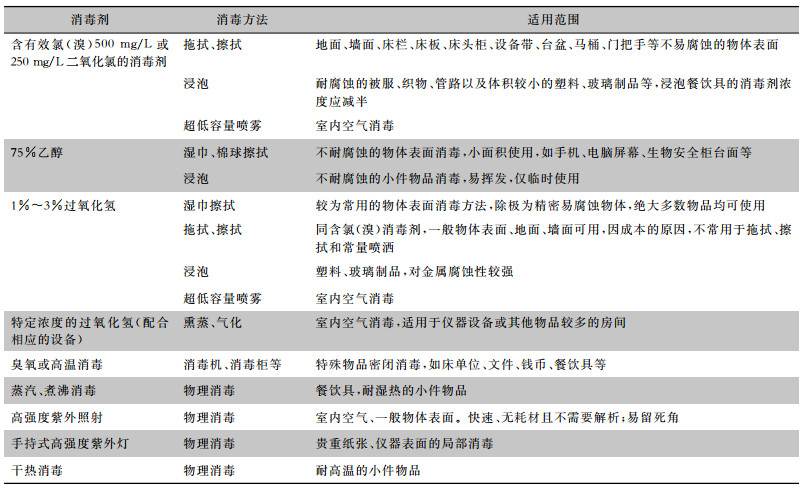
2.2 消毒方法的选择根据消毒对象的特点合理选择消毒方法和消毒剂,终末消毒通常以化学消毒为主,常见消毒剂、消毒方法及适用范围见表 1。
| 表 1 常用消毒剂、消毒方法适用范围 |
|
用蘸湿消毒剂的清洁布或地巾等拖、擦拭被消毒物体表面、地面,并保持湿润至规定消毒时间;所使用的消毒剂可能对消毒表面有腐蚀性时,消毒后用清水去除残留的消毒剂。高频接触表面推荐使用消毒湿巾进行擦拭消毒,更加便捷、易操作。
2.2.2 浸泡消毒将被消毒物品完全浸没于消毒剂内,至规定作用时间,然后用流动水去除残留的消毒剂。
2.2.3 喷雾消毒[8-9]包括常量喷雾和超低容量喷雾(气溶胶喷雾)。常量喷雾的雾滴较大,所形成的雾滴不能在空气中悬浮,只能用于大面积的环境物体表面消毒;超低容量喷雾雾滴粒径较小,通常在50 μm以下,雾滴能够长时间悬浮在空气中,可用于空气消毒和物体表面消毒,常用消毒剂包括二氧化氯、过氧化氢、次氯酸等,含氯(溴)消毒剂不能用于超低容量喷洒。
2.2.4 熏蒸、气化消毒通过配套设备将消毒剂的雾滴变得更细、粒径达到10 μm以下,使消毒剂弥散性更高,对表面的腐蚀性更低,如过氧化氢消毒机、过氧化氢消毒机器人,可用于空气消毒和物体表面消毒。
2.2.5 物理消毒方法包括开窗自然通风、紫外线照射、煮沸消毒、干热(蒸汽)消毒等。
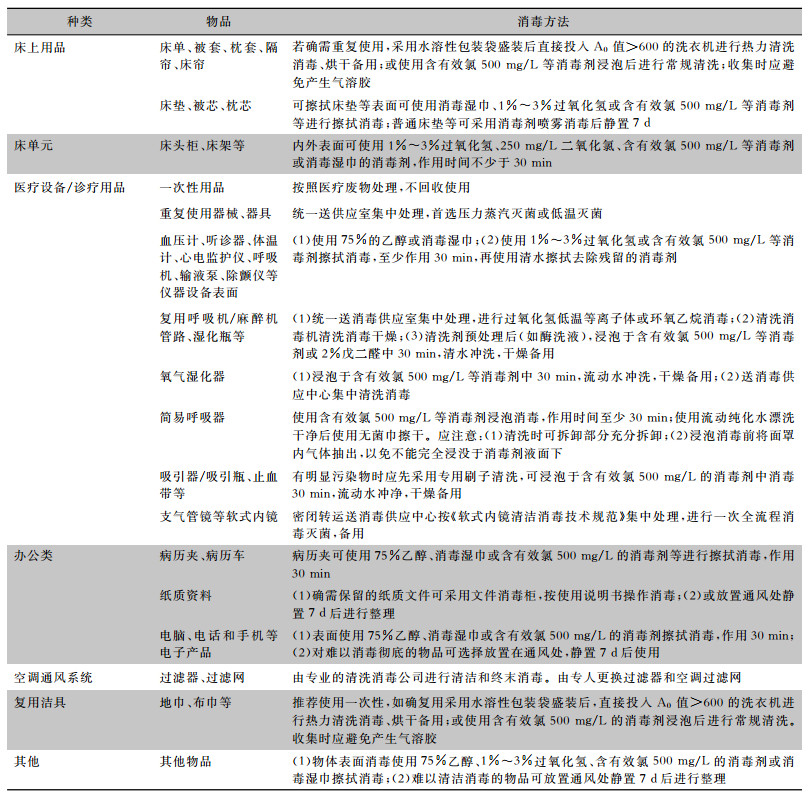
3 重点对象消毒方法对不同对象开展消毒,需要结合实际条件,选择适宜的消毒剂并按产品说明书的消毒方法开展消毒,原则上应在达到消毒效果的同时,尽量降低对环境、设备和人的影响,常用医疗用品及诊疗器械终末消毒方法见表 2。
| 表 2 常用医疗用品及诊疗器械终末消毒方法 |
|
首选开窗通风,必要时进行空气消毒。空气消毒时密闭房间,使用过氧化氢干雾、气溶胶终末消毒机(配合相应的过氧化氢消毒剂)、高强度紫外线灯进行空气消毒。空气消毒完毕、人进去前应先开窗通风或采取化学消毒剂降解处理[10]。
3.2 地面和物体表面有肉眼可见污染物时,应先完全清除污染物再消毒。可使用季铵盐消毒剂、含氯(溴)消毒剂、二氧化氯消毒剂擦拭、拖拭、喷洒消毒,作用30 min[2, 11]。如喷洒消毒,喷洒后应再擦拭/拖拭消毒。地面消毒先由外向内喷洒一次,喷药量为100~300 mL/m2, 待室内消毒完毕后,再由内向外重复喷洒一次,作用至消毒时间。喷洒消毒完成后,应由内向外再拖拭消毒一次。床、床头柜等内外表面采用消毒剂擦拭消毒。
3.3 医疗仪器设备、诊疗用品使用后的一次性医疗用品,均按照医疗废物集中处置。须外送消毒供应中心等集中进行消毒/灭菌的复用医疗仪器设备、诊疗用品,应先使用消毒剂擦拭、浸泡等预消毒,再外送常规清洗消毒。
3.4 办公用品和电子设备使用消毒湿巾擦拭消毒,或使用手持式高强度紫外灯照射,不建议使用喷洒消毒。
3.5 床垫、被芯、枕芯等如采用防水的床垫、被芯、枕芯,可采用消毒湿巾擦拭;如不防水,建议床垫、被芯、枕芯可采用消毒剂喷雾消毒[12]。
3.6 衣服、被褥、床单、被套等织物品确需回收使用者,无肉眼可见污染物时,可使用水溶性包装袋盛装后,按照感染性织物洗消流程,使用A0值>600的医用织物清洗消毒机进行热力清洗消毒;也可使用含氯消毒剂(有效氯含量为500 mg/L)等浸泡消毒后,再进行常规清洗干燥[12]。
3.7 餐(饮)具一次性餐(饮)具清除容器内残渣后,全部按照医疗废物处理。重复使用的餐(饮)具清除容器内残渣后,首选煮沸消毒或蒸汽消毒30 min。
3.8 地漏和下水使用含氯(溴)消毒剂或二氧化氯对所有地漏、下水道进行冲洗消毒。
3.9 纸质文件尽量不保留纸质文件,按照医疗废物集中处置。确需保留的纸质文件可采用文件消毒柜进行消毒或打包后环氧乙烷灭菌,少量贵重纸张也可使用高强度紫外灯照射消毒。
3.10 空调通风系统如在空调通风系统的管路安装空气消毒装置(等离子、高强度紫外线灯等),以保证空调管路内的空气经过消毒,可不对空调管路进行终末消毒[13]。集中空调通风系统应按照《公共场所集中空调通风系统清洗消毒规范》WS/T 396—2012[14],定期委托专业清洗消毒公司开展清洁和终末消毒;风机盘管空调和分体空调也建议委托空调清洗机构定期清洁和终末消毒。出/回风口格栅可采用擦拭消毒。用于风机盘管表面消毒的消毒剂应关注兼容性。
4 消毒过程质控所有终末消毒工作均应按照消毒工作方案对整个消毒操作过程进行过程评估。评估工作由所在医院/科室负责实施,一旦发现问题,应立即改进,并重新开展消毒工作。
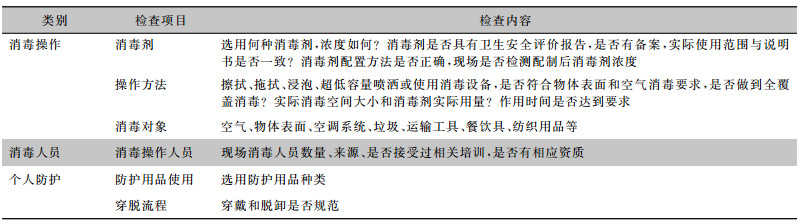
消毒过程评价主要包括但不限于消毒产品选择、消毒剂配制、消毒程序、消毒范围、消毒器械使用、个人防护等环节,评价人员通过现场参与或调阅监控的方法,结合相关消毒记录文件,开展过程评价并填写消毒过程评价表,消毒过程现场评价见表 3。
| 表 3 消毒过程现场评价表(参考) |
|
针对新冠病毒感染患者的环境终末消毒效果评价包括物体表面消毒效果评价和空气消毒效果评价。
4.1.1 空气消毒效果评价使用常规消毒方法无法清除病毒RNA,因此应使用自然菌杀灭率进行评价[15]。消毒前后用平板暴露法进行空气自然菌采样,参照《新冠肺炎疫情期间现场消毒评价标准》WS/T 774—2021进行布点和检测[16]。结果判断:自然菌平均杀灭率应≥90%,判为消毒合格;消毒前空气自然菌平均菌落数≤10 CFU/(皿·15 min),可不计算杀灭率,消毒后空气自然菌平均菌落数<4 CFU/(皿·15 min),判为消毒合格。
4.1.2 物体表面消毒效果评价使用指示微生物(金黄色葡萄球菌ATCC 6538和大肠埃希菌ATCC 8099)进行物体表面消毒效果评价。参照《新冠肺炎疫情期间现场消毒评价标准》WS/T 774—2021,选择患者高频接触的物体表面布点,放置指示微生物载体,在消毒因子难以达到的位置可以适当增加布点,试验标本总数不少于30个。指示微生物载体放置宜分散布点,具体布点位置需对现场消杀人员保密。结果判断:指示微生物平均杀灭率≥99.9%,且杀灭率≥99.9%的标本数占90%以上,判为消毒合格。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
Mannar D, Saville JW, Zhu X, et al. SARS-CoV-2 Omicron variant: antibody evasion and cryo-EM structure of spike protein-ACE2 complex[J]. Science, 2022, 375(6582): 760-764. DOI:10.1126/science.abn7760 |
| [2] |
Kasloff SB, Leung A, Strong JE, et al. Stability of SARS-CoV-2 on critical personal protective equipment[J]. Sci Rep, 2021, 11(1): 984. DOI:10.1038/s41598-020-80098-3 |
| [3] |
吴双胜, 张姣姣, 孙瑛, 等. 一起可能经气溶胶传播的新型冠状病毒Delta变异株聚集性疫情调查[J]. 中华流行病学杂志, 2022, 43(3): 305-309. Wu SS, Zhang JJ, Sun Y, et al. Survey of possible aerosol transmission of a COVID -19 epidemic caused by 2019-nCoV Delta variant[J]. Chinese Journal of Epidemiology, 2022, 43(3): 305-309. |
| [4] |
Kampf G, Todt D, Pfaender S, et al. Persistence of coronaviru-ses on inanimate surfaces and their inactivation with biocidal agents[J]. J Hosp Infect, 2020, 104(3): 246-251. DOI:10.1016/j.jhin.2020.01.022 |
| [5] |
Ratnesar-Shumate S, Williams G, Green B, et al. Simulated sunlight rapidly inactivates SARS-CoV-2 on surfaces[J]. J Infect Dis, 2020, 222(2): 214-222. DOI:10.1093/infdis/jiaa274 |
| [6] |
Cheng P, Chen WZ, Xiao SL, et al. Probable cross-corridor transmission of SARS-CoV-2 due to cross airflows and its control[J]. Build Environ, 2022, 218: 109137. DOI:10.1016/j.buildenv.2022.109137 |
| [7] |
Wang YX, Liu ZJ, Liu HY, et al. Droplet aerosols transportation and deposition for three respiratory behaviors in a typical negative pressure isolation ward[J]. Build Environ, 2022, 219: 109247. DOI:10.1016/j.buildenv.2022.109247 |
| [8] |
Amoah AGB, Sagoe KW, Quakyi IA, et al. Further observations on hydrogen peroxide antisepsis and COVID -19 cases among healthcare workers and inpatients[J]. J Hosp Infect, 2022, 126: 103-108. DOI:10.1016/j.jhin.2022.05.007 |
| [9] |
Alnimr A, Alamri A, Salama KF, et al. The environmental deposition of severe acute respiratory syndrome coronavirus 2 in nosocomial settings: role of the aerosolized hydrogen pero-xide[J]. Risk Manag Healthc Policy, 2021, 14: 4469-4475. DOI:10.2147/RMHP.S336085 |
| [10] |
Ghoroghi A, Rezgui Y, Wallace R. Impact of ventilation and avoidance measures on SARS-CoV-2 risk of infection in public indoor environments[J]. Sci Total Environ, 2022, 838(Pt 4): 156518. |
| [11] |
国务院应对新型冠状病毒肺炎疫情联防联控机制综合组. 关于进一步优化进口物品新冠肺炎疫情防控工作的通知: 国卫明电(2022)270号[EB/OL]. (2022-07-12)[2022-08-25]. http://www.nhc.gov.cn/xcs/gzzcwj/202207/7602660406c24d5d96d8d9377ba2157e.shtml. Comprehensive Group of Joint Prevention and Control Mechanism of the State Council in Response to coronavirus disease 2019. Notice on further optimizing the prevention and control of COVID -19 in imported goods, (2022)270[EB/OL]. (2022-07-12)[2022-08-25]. http://www.nhc.gov.cn/xcs/gzzcwj/202207/7602660406c24d5d96d8d9377ba2157e.shtml. |
| [12] |
Virtanen J, Aaltonen K, Kivistö I, et al. Survival of SARS-CoV-2 on clothing materials[J]. Adv Virol, 2021, 2021: 6623409. |
| [13] |
Ueki H, Ito M, Furusawa Y, et al. A 265-nanometer high-power deep-UV light-emitting diode rapidly inactivates SARS-CoV-2 aerosols[J]. mSphere, 2022, 7(2): e0094121. DOI:10.1128/msphere.00941-21 |
| [14] |
中华人民共和国卫生部. 公共场所集中空调通风系统清洗消毒规范: WS/T 396-2012[S]. 北京: 中国标准出版社, 2013. Ministry of Health of the People's Republic of China. Specification of cleaning and disinfecting for central air conditioning ventilation system in public buildings: WS/T 396-2012[S]. Beijing: Standards Press of China, 2013. |
| [15] |
南征, 周妍妍, 苏建荣, 等. 不同消毒方式对流感病毒RNA消除效果的研究[J]. 中国消毒学杂志, 2022, 39(6): 410-413. Nan Z, Zhou YY, Su JR, et al. Efficacy of various disinfection methods on elimination of influenza virus RNA[J]. Chinese Journal of Disinfection, 2022, 39(6): 410-413. |
| [16] |
中华人民共和国国家卫生健康委员会. 新冠肺炎疫情期间现场消毒评价标准: WS/T 774-2021[S]. 北京: 中国标准出版社, 2021. National Health Commission of the People's Republic of China. Standard of field disinfection evaluation during COVID -19 epidemic: WS/T 774-2021[S]. Beijing: Standards Press of China, 2021. |



