2. 复旦大学附属中山医院感染管理科,上海 200032;
3. 上海市徐汇中学,上海 200030;
4. 上海市行知中学,上海 201900
2. Department of Infection Management, Zhongshan Hospital, Fudan University, Shanghai 200032, China;
3. Shanghai Xuhui High School, Shanghai 200030, China;
4. Shanghai Xingzhi High School, Shanghai 201900, China
随着外科微创手术的发展,越来越多的复杂医疗器械应用于各类手术中,此类手术器械的有效清洁和灭菌监管难度也越来越大[1]。部分手术器械由于材质特殊、构造复杂、价格昂贵而无法广泛购买,为此器械供应商将这些手术器械租借给医院重复使用,在手术结束后、供应商回收前需彻底清洗这些外来手术器械[2],以减少残留的血迹、污染物,避免医院获得性感染的发生[3]。视觉上的清洁是当前判定手术器械清洗效果的主要方法之一,也是清洗是否合格的最低标准[4-5]。管腔类器械在缺乏检测设备的情况下,无法对其内部已形成的划痕、内层剥离、碎片和液体残留等进行有效查明,受损的内壁通道有利于细菌的黏附和隐藏,并最终形成难以清除的生物膜,因而是当前感染防控的盲点之一。
管腔可视化检测系统作为检查内镜、管腔器械通道的可视化检查系统,其纤细的导线可以进入内镜手柄的开口处或管腔器械的狭长通道,进行可视化检查[6],探明内镜/管腔器械内部异物残留和污染情况。本研究采用可视化的腔镜通道检查系统,深入研究某院外来医疗器械管腔结构的脊柱手术器械的清洗质量,以期发现此类手术器械清洗的难点,为开发针对性解决方案,改进清洗质量控制体系,进一步完善和优化处理流程提供参考。
1 对象与方法 1.1 检测对象2021年9—10月某院所接收的外来脊柱手术器械,从中选取带管腔或中空结构的器械共计291件,其中椎间孔镜器械137件,包括脊柱把持器、脊柱撑开器、穿针、扩张器、导管、工作套筒、咬骨钳、半柔性抓钳、髓核钳、篮钳、外鞘等,普通脊柱手术管腔结构器械154件,包括钉起子套筒、植骨漏斗、人工椎体安装套筒、颈椎提拉器、颈前持取器、假体持取器、腰颈椎抗扭套筒、扭力扳手对抗套筒、TPAL试模持取器、蛙式复位钳、经皮套筒、把持器外套筒、枪式复位钳、万向钉植入器套筒、固定钉植入器套筒、植骨器、腰椎复位套筒、融合器把持器、T型扭力手柄、直型快装手柄、T型快装手柄等。椎间孔镜器械使用时长约为半年至3年不等,其他脊柱手术器械均在各医院间流转使用,使用时长未知。存在管腔结构的器械:常规在含酶液中手工刷洗再采用全自动清洗机清洗; 结构复杂或污渍残留的器械:使用含酶清洗液浸泡后手工刷洗,生锈器械进行超声除锈处理。
1.2 材料和设备腔镜通道检查系统(上海锐净)、医用清洗剂(Steris公司),超声清洗机(宁波科生),压力水枪、压力气枪(新华医疗)医用含酶清洗液。
1.3 检测方法所有器械均在接收时、完成清洗后进行腔镜系统检查。检测时,根据器械孔径大小将腔镜通道检查系统的导线(外径1.8 mm或2.2 mm) 插入器械管腔内实时检查,将捕获视频或静止图像通过软件呈现在电脑显示屏上,记录每件器械内壁检测结果。
1.4 结果判断管腔器械内壁若出现血渍、锈渍、异物、污渍、组织残留,则判断为污染。
1.5 统计学方法将检测结果录入Excel软件,应用SPSS 22.0进行统计分析。计数资料的比较采用χ2检验,以P≤0.05为差异有统计学意义。
2 结果 2.1 器械结构291件管腔器械中,一端为封闭盲端的50件,两端开口的241件; 149件器械内表面具有凹陷或者突起的设计结构(其中50件带盲端,99件两端开口),142件器械内表面平滑(均为两端开口)。
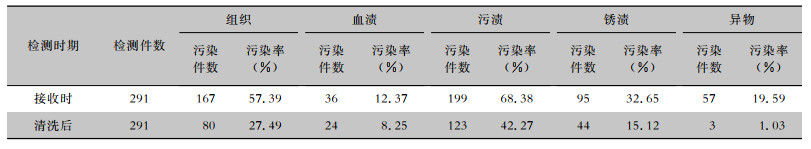
2.2 污染物残留情况腔镜通道检查系统检测显示,291件管腔器械,接收时污染率为89.69%(261件),清洗后污染率为59.45%(173件),两者比较差异有统计学意义(χ2=70.168,P<0.001)。接收时的主要污染物为污渍、组织、锈渍,见图 1。接收时污渍、组织、锈渍污染率分别为68.38%、57.39%、32.65%,清洗后污渍、组织、锈渍污染率仍较高,分别为42.27%、27.49%、15.12%,见表 1。
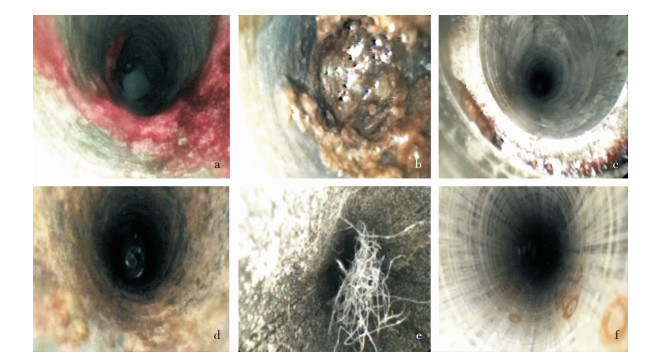 |
| 注:a、b为组织,c为血渍,d为污渍,e为异物,f为锈渍。 图 1 管腔型脊柱手术器械内表面的污染物图像 Figure 1 Contaminants on the inner surface of luminal spinal surgical instruments |
| 表 1 管腔器械清洗前后污染物污染情况 Table 1 Contamination of contaminants before and after cleaning of luminal instruments |
|
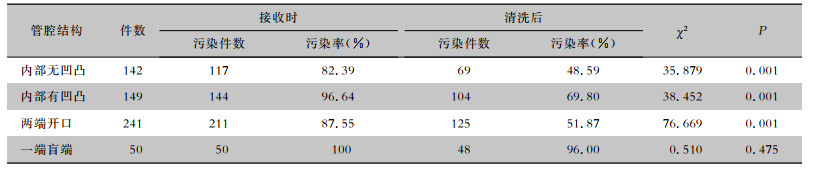
内部无凹凸的管腔器械接收时和清洗后的污染率分别为82.39%、48.59%,内部有凹凸的管腔器械接收时和清洗后的污染率分别为96.64%、69.80%,两端开口的管腔器械接收时和清洗后的污染率分别为87.55%、51.87%,接收时与清洗后污染率比较,差异均具有统计学意义(均P<0.05);仅一端开口的管腔器械接收时和清洗后污染率分别为100%、96.00%,接收时与清洗后污染率比较,差异无统计学意义(P>0.05)。见表 2。
| 表 2 不同结构管腔器械清洗前后污染物污染情况 Table 2 Contamination of contaminants of different structure luminal instruments before and after cleaning |
|
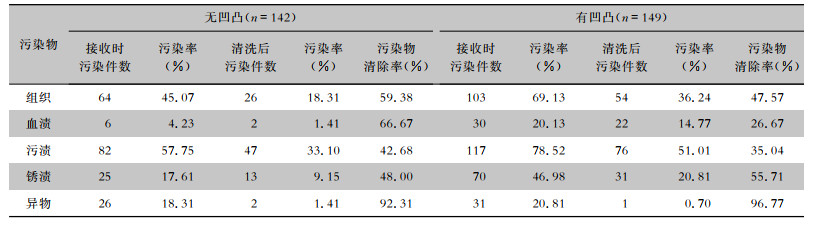
无凹凸的管腔器械对组织、血迹、污渍、锈迹和异物的清除率分别为59.38%、66.67%、42.68%、48.00%、92.31%,有凹凸的管腔器械内壁上残留的组织、血迹、污渍、锈迹和异物的清除率分别为47.57%、26.67%、35.04%、55.71%、96.77%。见表 3。
| 表 3 管腔器械不同内壁结构各污染物污染情况及清除效果 Table 3 Contamination and removal effect of contaminants in different inner wall structures of luminal instruments |
|
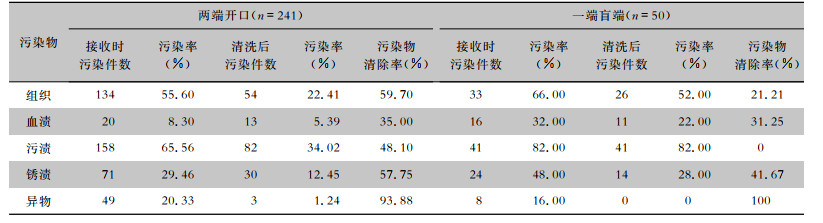
两端开口的管腔器械内壁残留的组织、血渍、污渍、锈渍和异物的清除率分别为59.70%、35.00%、48.10%、57.75%、93.88%,一端开口的管腔器械内壁残留的组织、血渍、污渍、锈渍和异物的清除率分别为21.21%、31.25%、0、41.67%、100%。见表 4。两端开口的管腔器械组织和污渍的清除率均高于一端盲端,差异均有统计学意义(χ2分别为15.718、31.907,均P<0.001);血渍、锈渍、异物清除率,两端开口的管腔器械与一端盲端的管腔器械比较,差异均无统计学意义(均P>0.05)。
| 表 4 管腔器械不同端口结构污染物污染情况及清除效果 Table 4 Contamination and removal effect of contaminants at different end structures of luminal instruments |
|
《医院消毒供应中心第1部分:管理规范》WS 310.1—2016行业标准[7]规定,可复用医疗手术器械的清洗、消毒、灭菌统一由医院消毒供应中心(central sterile supply department,CSSD)负责; 并进一步加强了外来医疗器械的管理要求,如择期手术使用的外来医疗器械需提前1 d送达CSSD,再处理需要遵循厂家说明书; 使用后的外来医疗器械应由CSSD清洗消毒后方可交器械供应商。管腔器械的外表面容易清洗干净,也易于观察,而管腔器械由于孔径较小,内壁缺乏有效的可视化检查手段,其清洗和监测一直是CSSD工作的难点之一。
本研究所涉及的脊柱手术外来医疗器械大多是在各医院间流转使用,各级医院CSSD的清洗消毒质量差异较大。此外,随着微创手术技术的飞速发展,外来医疗器械中很多器械的结构需借助卡口将不同的器械组件进行连接,这些凹凸不平的设计导致其内壁比无凹凸的器械更难清洗,污染物更易残留。预研究时发现,新接收的外来医疗器械清洗质量堪忧,但既往较少有研究关注。本研究采用腔镜通道检查系统较为深入的观察脊柱手术外来医疗器械管腔结构的内壁并评估清洗效果,其细长的检查器导线可以深入到管腔器械内部检查清洗质量,同时可以观察到脊柱手术器械的内壁结构的差异,具有较强的应用价值。多个协会最近发布的指南也建议在内镜护理和再处理期间对工作通道进行目视检查[8-9]。
本研究发现,带有盲端的器械比两端开口的器械更难清洗,更容易残留组织和污渍,其污染物清除率仅为21.21%和0,有凹凸的器械比无凹凸的器械更容易残留血渍和污渍。部分器械同时存在干涸的血渍、污渍,锈渍等问题,多与长时间清洗质量不合格有关。尽管《医院消毒供应中心行业规范第3部分:清洗消毒及灭菌效果监测标准》WS 310.3—2016[10]要求采用目测和带光源放大镜检查每件器械,保证器械无血渍、污渍、水垢等残留物质和锈斑,清洗质量不合格者应重新处理。但大多数管腔器械存在手术后没有及时处理,也没有及时进行保湿处置等问题,长时间缺乏监管并在多个医疗机构流转,最终导致各种清洗不合格情况[3]。提示结构复杂的管腔器械的清洗必须关注其内部的结构,并根据不同的结构设计不同的清洗方案[11],或使用针对性的清洗设备以保证清洗质量[12]。
此外,脊柱手术外来医疗器械由于其材质特殊、结构复杂,在灭菌的过程中可能存在升温延迟的现象[13]。一些血液和体液的残留可为内壁残留的细菌提供营养物质,导致生物膜缓慢的形成[14-15],增加灭菌的难度[16]。因此,未来需要进一步改进和优化管腔类手术器械的处理流程。对于不能进行及时清洗的管腔类手术器械,应进行保湿等预处理; 接收时,应检查管腔类手术器械内部污染物情况; 清洗后应加强清洗质量的检查,避免污染严重的器械进入手术操作中。
本研究也存在一定的局限:腔镜通道检查系统为目测法的拓展,仅能定性评估各器械的清洗质量,且未结合ATP生物荧光检测或蛋白残留试验等进行半定量评估,因而限制结果的外推。未来将结合腔镜通道检查系统和蛋白残留定量研究,以进一步评价手术器械的清洗质量。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
Ling ML, Ching P, Widitaputra A, et al. APSIC guidelines for disinfection and sterilization of instruments in health care facilities[J]. Antimicrob Resist Infect Control, 2018, 7: 25. DOI:10.1186/s13756-018-0308-2 |
| [2] |
Alfa MJ. Medical instrument reprocessing: current issues with cleaning and cleaning monitoring[J]. Am J Infect Control, 2019, 47S: A10-A16. |
| [3] |
Huang YD, Huang Y, Chen YH, et al. Factors affecting implementation and pass rates of surgical instrument moistening[J]. BMC Infect Dis, 2021, 21(1): 752. DOI:10.1186/s12879-021-06471-3 |
| [4] |
Association for the Advancement of Medical Instrumentation. Comprehensive guide to steam sterilization and sterility assu-rance in health care facilities, amendment 4: ANSI/AAMI ST79: 2010/A4[S]. American National Standard, 2014.
|
| [5] |
World Health Organisation. Decontamination and reprocessing of medical devices for health-care facilities[EB/OL]. [2022- 03-10]. https://apps.who.int/iris/bitstream/handle/10665/250232/9789241549851-eng.pdf;sequence=1.
|
| [6] |
Thaker AM, Kim S, Sedarat A, et al. Inspection of endoscope instrument channels after reprocessing using a prototype borescope[J]. Gastrointest Endosc, 2018, 88(4): 612-619. DOI:10.1016/j.gie.2018.04.2366 |
| [7] |
中华人民共和国国家卫生和计划生育委员会. 医院消毒供应中心第1部分: 管理规范: WS 310.1—2016[S]. 北京: 中国标准出版社, 2017. National Health and Family Planning Commission of the People's Republic of China. Central sterile supply department(CSSD)-part 1: management standard: WS 310.1-2016[S]. Beijing: Standards Press of China, 2017. |
| [8] |
Liu TC, Peng CL, Wang HP, et al. SpyGlass application for duodenoscope working channel inspection: impact on the microbiological surveillance[J]. World J Gastroenterol, 2020, 26(26): 3767-3779. DOI:10.3748/wjg.v26.i26.3767 |
| [9] |
Kaneoka A, Krisciunas GP, Walsh K, et al. A comparison of 2 methods of endoscopic laryngeal sensory testing: a preliminary study[J]. Ann Otol Rhinol Laryngol, 2015, 124(3): 187-193. DOI:10.1177/0003489414550241 |
| [10] |
中华人民共和国国家卫生和计划生育委员会. 医院消毒供应中心第3部分: 清洗消毒及灭菌效果监测标准: WS 310.3—2016[S]. 北京: 中国标准出版社, 2017. National Health and Family Planning Commission of the People's Republic of China. Central sterile supply department(CSSD)-part 3: surveillance standard for cleaning, disinfection and sterilization: WS 310.3-2016[S]. Beijing: Stan-dards Press of China, 2017. |
| [11] |
Gul M, Ghafoor R, Aziz S, et al. Assessment of contamination on sterilised dental burs after being subjected to various pre-cleaning methods[J]. J Pak Med Assoc, 2018, 68(8): 1188-1192. |
| [12] |
张萍, 梁东竹, 王春华, 等. 新型真空超声清洗器清洗及干燥效果评价[J]. 中国医学装备, 2021, 18(6): 195-198. Zhang P, Liang DZ, Wang CH, et al. Observational study on the effects of cleanness and dryness of new type of vacuum ultrasonic cleaner[J]. China Medical Equipment, 2021, 18(6): 195-198. DOI:10.3969/J.ISSN.1672-8270.2021.06.049 |
| [13] |
袁园, 刘作辉. 不同脉动形式对外来器械蒸汽灭菌升温延迟的研究[J]. 中国消毒学杂志, 2020, 37(6): 428-430. Yuan Y, Liu ZH. Study on the heating delay of steam sterilization of loaner instruments with different pulsations[J]. Chinese Journal of Disinfection, 2020, 37(6): 428-430. |
| [14] |
Evangelista SDS, Guimaraes NR, Garcia NB, et al. Effectiveness of manual versus automated cleaning on Staphylococcus epidermidis biofilm removal from the surface of surgical instruments[J]. Am J Infect Control, 2020, 48(3): 267-274. DOI:10.1016/j.ajic.2019.08.024 |
| [15] |
Zhou WZ, Ye C, Huang XQ, et al. Efficacy of cleaning me-thods for ophthalmic microscopic instruments: a comparison study[J]. AORN J, 2020, 112(2): 112-121. DOI:10.1002/aorn.13105 |
| [16] |
Davies D. Understanding biofilm resistance to antibacterial agents[J]. Nat Rev Drug Discov, 2003, 2(2): 114-122. DOI:10.1038/nrd1008 |



