新型冠状病毒肺炎(简称新冠肺炎)是2019年12月在武汉首先发现的一种新传染病[1],经实验室基因检测和病毒分离确定为新型冠状病毒[2](severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)[3]感染所致。主要经呼吸道飞沫传播和接触传播,人群普遍易感[4],全球已有100多个国家和地区发现确诊病例。目前认为,新冠肺炎传染源主要是新冠肺炎患者,且隐性感染者(即无症状感染者)也可能成为传染源[5]。为了解新冠肺炎病例密切接触者感染情况,同时避免疫情进一步扩散,特对本地区738例医学观察人员进行了血常规和鼻咽拭子的新型冠状病毒核酸检测(简称核酸检测),现将结果报告如下。
1 资料与方法 1.1 资料来源选取2020年2月11—23日某定点隔离酒店内738例新冠肺炎病例密切接触且无明显临床症状的医学观察人员,以新冠肺炎病例家庭成员为主,其中男性376例,女性362例。年龄为7个月~91岁。
1.2 仪器与试剂核酸检测使用中山大学达安基因的Smart32型核酸提取仪和配套的扩增试剂,以及杭州安杰思医学科技股份有限公司的AFD4800型实时荧光定量分析仪;血常规检测使用希森美康XN-1000型全自动血液分析仪及原厂试剂、校准品和质控品。
1.3 方法 1.3.1 采样方法医学观察人员均为单间隔离,于酒店独立房间内采集观察人员血常规及鼻咽拭子标本。鼻咽拭子采样时,采样人员一手轻扶被采集人员的头部,一手执拭子,拭子贴鼻孔进入,沿下鼻道的底部向后缓缓深入,由于鼻道呈弧形,不可用力过猛,以免发生外伤出血。待拭子顶端到达鼻咽腔后壁时,轻轻旋转一周(如遇反射性咳嗽,应停留片刻),然后缓缓取出拭子,将拭子头浸入装有2 mL裂解液(与核酸提取试剂盒中裂解液相同)的标本采集管或含RNA酶抑制剂的细胞保存液中,插入拭子后在靠近顶端处折断无菌拭子杆,旋紧管盖并用封口膜封闭[6-7]。
1.3.2 检测方法鼻咽拭子标本进行核酸检测,严格依照仪器、试剂说明书要求进行;血常规使用自动进样模式进行检测。
1.3.3 核酸检测结果判读(1) 当ORF1ab和N基因同时呈阳性时,或者若仅ORF1ab或N基因其中之一的检测结果呈阳性时,需重新提取原标本的核酸进行复查,复查后ORF1ab或N基因仍显示为阳性时[8],则可判定为阳性。(2)当出现以下两种情况时为“可疑”:①2个位点的Ct值位于阳性Ct值和阴性Ct值之间或其中1个位点判读为阳性,另1个位点的Ct值位于阳性Ct值和阴性Ct值之间(具体请参考试剂盒说明书);②2个位点中的1个位点为阴性,另1个位点的Ct值位于阳性Ct值和阴性Ct值之间。对于“可疑”阳性结果,建议重新对标本进行核酸提取,并与该标本前一次提取的核酸同时扩增检测,结合两次检测,2个位点可判断为“阳性”则可报告“阳性”,否则应报告“可疑”[7]。(3)当两个位点扩增结果无反应,可报告“阴性”,并对结果进行解释,此情况可能是病毒载量低于阳性限,应结合临床分析[7]。
1.3.4 复检要求核酸检测结果可疑者需隔日重新采样复测。
1.3.5 分析方法对所有血常规和核酸检测结果进行统计分析,计算无症状感染者比例及血常规结果符合新冠肺炎发病早期特点占比。
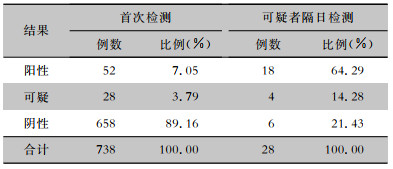
2 结果 2.1 核酸检测结果738例新冠肺炎病例密切接触医学观察者核酸检测阳性70例(9.49%),阴性664例(89.97%),可疑4例(0.54%)。各年龄段阳性率为7个月~6岁12.50%(2/16),7~14岁10.34%(3/29),15~40岁9.00%(19/211),41~60岁8.09%(25/309),>61岁12.14%(21/173)。阳性结果来源于23个家庭,家庭内核酸检测阳性者1~6例,中位数为3例,主要呈家庭聚集性分布。核酸检测结果见表 1。
| 表 1 医学观察者首次核酸检测及可疑者隔日复测结果 Table 1 Results of the initial nucleic acid test of medical observed persons and the retest of suspected persons the next day |
|
738例医学观察者血常规检测,白细胞计数减少者(<3.5×109/L)2例,淋巴细胞计数减少者(<1.1×109/L)21例,核酸检测结果阳性及可疑医学观察者血标本白细胞计数均正常,仅2例淋巴细胞计数减少。无症状感染者血常规结果符合新冠肺炎发病早期特点者仅占2.70%(2/74,包含4例仍可疑者)。
2.3 发病情况70例核酸检测结果阳性者,42.86%(30例)于14 d观察期内出现发热、咳嗽、气促、呼吸困难等症状,被列为确诊病例转至定点医院。后续对余下40例送至指定隔离点继续观察,超过14 d后有2例发病,余下38例全部转阴。664例核酸检测阴性者,1.51%(10例)于14 d观察期内出现症状,并被临床确诊(未在本院再次进行核酸检测),余下阴性观察者至14 d期满均无发病情况,且第二次核酸检测也均为阴性。4例可疑医学观察者平稳度过14 d观察期,随后送至指定隔离点继续观察,后续全部转阴。14天内发病率为5.42%(40/738),继续观察期发病率为4.55%(2/44),整个集中隔离期发病率为5.69%(42/738)。
3 讨论新冠肺炎已证实可以在人际间传播[9],且人群普遍易感,导致目前感染病例仍在增长,已出现家庭聚集性发病[10],并形成全球蔓延态势。世界卫生组织于2020年1月31日宣布新冠肺炎疫情暴发构成“国际关注的突发公共卫生事件(public health emergency of international concern,PHEIC)”[11-12]。当前研究表明,无症状新型冠状病毒感染者可能造成疾病传播[13],故早期识别对控制疾病的流行与传播极为重要[14]。
对738例以新冠肺炎病例家庭成员为主的无症状医学观察人员进行核酸检测筛查,阳性率高达9.49%,考虑到实际感染患者的核酸检测不一定为阳性,本研究中核酸检测呈阴性的受检者在观察期内也有发病的情况,实际感染的比例应该更高。70例核酸检测阳性但暂无症状者,45.71%在30 d内转化为确诊病例,这些转化病例在检测核酸时病毒已侵入体内,只是尚未引起全身免疫性反应,但也可能具有一定的传染性。因此,尽早发现无症状感染者有利于提前干预,避免或缩短病程,减轻症状,也有助于疫情防控[15]。
研究发现,部分新冠肺炎潜伏期>14 d[16],故将14 d内未发病的核酸检测阳性和可疑医学观察者转移至特定隔离点继续观察,后续确有发病的情况;其他观察者在整个医学观察期均未发病,目前已全部转阴并解除集中隔离(集中隔离时间最长者为27 d)。
各项规范、指南、专家共识明确指出,核酸检测阴性,并不能排除被新型冠状病毒感染的可能。本研究中有核酸检测呈阴性的医学观察者在14 d观察期内出现临床症状而被临床确诊的情况。而余下核酸检测阴性医学观察者则平稳度过了14 d的隔离观察期,并在第二次核酸检测中仍呈阴性,随即解除定点隔离,并嘱咐不适随诊(至截稿日尚未接到任何不适消息报告)。因此,依据本研究检测结果,隔离14 d后核酸检测仍呈阴性的密切接触者基本可排除被新型冠状病毒感染的可能。
为做好疫情的排查,国家卫生健康委员会指出无症状感染者主要来源有:(1)新冠肺炎病例的密切接触者;(2)聚集疫情调查中的主动检测;(3)新冠肺炎病例传染源追踪过程中发现暴露人群;(4)有新冠肺炎病例、持续传播地区旅游史和居住史的人群。本研究仅以新冠肺炎病例的密切接触者为研究对象,目前尚未涉及其他3种无症状感染者,后期根据情况再做相应报道。
| [1] |
李六亿, 吴安华. 新型冠状病毒医院感染防控常见困惑探讨[J]. 中国感染控制杂志, 2020, 19(2): 105-108. |
| [2] |
Zhu N, Zhang D, Wang W, et al. A novel coronavirus from patients with pneumonia in China, 2019[J]. N Engl J Med, 2020, 382(8): 727-733. |
| [3] |
李宝林, 李芹, 吴刚, 等. 15例COVID-19患者治疗后痰、粪便标本新型冠状病毒核酸检测结果比较[J]. 中国感染控制杂志, 2020, 19(3): 239-244. |
| [4] |
中华人民共和国国家卫生健康委员会.新型冠状病毒感染的肺炎治疗方案(试行第七版)[EB/OL].[2020-03-04]2020-03-14].http://www.nhc.gov.cn/yzygj/s7653p/202003/46c9294a7dfe4cef80dc7f5912eb1989.shtml.
|
| [5] |
中华预防医学会新型冠状病毒肺炎防控专家组. 新型冠状病毒肺炎流行病学特征的最新认识[J]. 中华流行病学杂志, 2020, 41(2): 139-144. |
| [6] |
中华人民共和国国家卫生健康委员会.临床微生物学检验标本的采集和转运: WS/T 640-2018[S].北京, 2018.
|
| [7] |
中华医学会检验医学分会. 新型冠状病毒肺炎病毒核酸检测专家共识[J]. 中华医学杂志, 2020, 100(00): E003-E003. DOI:10.3760/cma.j.issn.0376-2491.2020.0003 |
| [8] |
中华人民共和国国家卫生健康委员会.新型冠状病毒感染的肺炎实验室检测技术指南(第二版)[EB/OL]. (2020-01-22)[2020-02-28]. http://www.nhc.gov.cn/xcs/zhengcwj/202001/c67cfe29ecf1470e8c7fc47d3b751e88.shtml.
|
| [9] |
南玲, 陈萍, 刘莎, 等. 新型冠状病毒肺炎疫情期间个人防护用品穿脱技能培训学习曲线分析[J]. 中国感染控制杂志, 2020, 19(3): 271-273. |
| [10] |
朱耐伟, 赵平, 戚中田. 2019新型冠状病毒肺炎治疗研究现状[J]. 中华微生物学和免疫学杂志, 2020, 40(1): 7-10. |
| [11] |
WHO. Statement on the second meeting of the International Health Regulations (2005) Emergency Committee regarding the outbreak of novel coronavirus (2019-nCoV)[EB/OL]. (2020-01-30)[2020-02-30] https://www.who.int/news-room/detail/30-01-2020-statement-on-the-second-meeting-of-the-international-health-regulations-(2005)-emergency-committee-regarding-the-outbreak-of-novel-coronavirus-(2019-ncov).
|
| [12] |
高占成.科学认识和科学管理是防控和救治新型冠状病毒肺炎的关键[J/OL].中华结核和呼吸杂志, 2020, 43(2020-02-05).http://rs.yiigle.com/yufabiao/1179588.htm. DOI: 10.3760/cma.j.issn.1001-0939.2020.0001.
|
| [13] |
高文静, 李立明. 新型冠状病毒肺炎潜伏期或隐性感染者传播研究进展[J]. 中华流行病学杂志, 2020, 41(4): 485-488. |
| [14] |
沈银忠, 卢洪洲. 提高对新型冠状病毒感染诊治的认识[J]. 中华传染病杂志, 2020, 38(1): 6-8. |
| [15] |
苑伟, 陈相军, 黄应德, 等. 某大型综合医院发热门诊1770例发热患者临床资料分析[J]. 中国感染控制杂志, 2020, 19(3): 277-280. |
| [16] |
Wang P, Lu JA, Jin YY, et al. Epidemiological characteristics of 1212 COVID-19 patients in Henan, China[J]. medRxiv preprint 2020. DOI: 10.1101/2020.02.21.20026112.
|



