2. 南京医科大学第一附属医院感染管理办公室, 江苏 南京 210029;
3. 南京医科大学附属江苏盛泽医院院长办公室, 江苏 苏州 215228
2. Healthcare-associated Infection Management Office, The First Affiliated Hospital with Nanjing Medical University, Nanjing 210029, China;
3. Hospital President's Office, Jiangsu Shengze Hospital with Nanjing Medical University, Suzhou 215228, China
随着近代科技的发展,二十世纪60年代光学纤维应用于内镜结构,使得内镜诊疗技术得到飞速发展,作为医生眼、手的延伸,已经达到了“无孔不入”的境界[1]。由于其材质特殊、结构复杂、精密度高,使用后清洗、消毒非常困难,微生物在内镜管道内形成生物膜的能力很强,可导致内镜清洗消毒的失败[2]。国外有研究[3-4]表明,使用后的内镜病原微生物载量为105~1010 CFU/mL,是感染传播的潜在危险因素,防止交叉感染是21世纪内镜检查面临的重大问题。从2000年开始已出现多次因内镜污染而造成的病原菌感染暴发流行[5],部分内镜甚至检出多重耐药菌,如耐碳青霉烯类肠杆菌(CRE)[6],多重耐药铜绿假单胞菌(MDR-PA)[7]。消毒效果监测是评价清洗消毒程序是否落实到位、自动清洗消毒设备是否正常运转,清洗消毒效果是否达标的重要手段[8]。2016年卫生行业标准《软式内镜清洗消毒技术规范》(WS 507—2016)[9]颁布以来,大多数医院对使用滤膜法检测内镜清洗消毒效果的关注提升,少数医院已经开始启用滤膜法,但因为考虑其检测效果、经济成本等问题,多数医院仍未开始实施。国内尚缺乏针对滤膜法和涂抹法检测内镜清洗消毒效果以及费用成本的研究,本研究通过分析某大型三级甲等综合医院2018年1—12月内镜检测结果,分析滤膜法和涂抹法检测内镜清洗消毒效果及成本对比,为其他医院提供借鉴。
1 资料与方法 1.1 资料来源随机抽取某大型三甲综合医院2018年1—12月清洗消毒后内镜,同一内镜分别通过滤膜法和涂抹法检测内镜清洗消毒效果。排除仅使用滤膜法或涂抹法其中一种方法检测的结果及受到污染的检测结果。同时利用问卷星与微信平台对部分医院内镜清洗消毒效果检测方法等情况进行问卷调查。
1.2 研究方法 1.2.1 数据收集将内镜分为胃镜、肠镜、纤支镜、胆道镜、鼻咽镜5类,分别统计使用滤膜法和涂抹法检测清洗消毒后合格率、病原菌检出率、菌落计数、成本消耗,并进行对比分析。利用问卷星与微信平台对部分医院内镜清洗消毒效果检测方法等情况进行调查,自主设计的调查问卷导入问卷星,自动形成二维码,发至院感微信群,各医院通过手机扫描二维码进行在线填写提交,统一进行分析。
1.2.2 采样方法根据《医院消毒卫生标准》(GB 15982—2012)[10]要求,取清洗消毒后内镜,采用无菌注射器抽取50 mL含相应中和剂的洗脱液,从活检口注入冲洗内镜管路,并全量收集并送检。
1.2.3 检测培养方法涂抹法:将洗脱液充分混匀,取洗脱液1.0 mL匀液于2个凝固的营养琼脂平皿,(36±1)℃恒温箱培养48 h;滤膜法(见图 1):将剩余洗脱液(49.0 mL)在无菌条件下采用滤膜(0.45 μm)过滤浓缩,将滤膜置于凝固的营养琼脂平皿上,置于(36±1)℃恒温箱培养48 h,计算菌落数。结果计算:当滤膜上的菌落可计数时:内镜上总菌落数(CFU/件)=两平行平皿的平均菌落数+滤膜上菌落数;当滤膜上的菌落不可计数时,菌落总数(CFU/件)=两平行平皿的平均菌落数×50。合格率=菌落数合格内镜数/采样内镜数×100%;检出率=培养出菌落的内镜数/采样内镜数×100%。
 |
| 图 1 六联抽滤系统示意图 Figure 1 Schematic diagram of six-chain suction filtration system |
根据《医院消毒卫生标准》(GB 15982—2012)和《软式内镜清洗消毒技术规范》(WS 507—2016)要求,消毒内镜合格标准:菌落总数≤20 CFU/件。
1.3 成本核算 1.3.1 增加的经济成本滤膜法耗材比涂抹法多,会增加一定的经济成本,包括:抽滤系统和滤膜(津市津腾实验设备有限公司);75%乙醇消毒剂(500 mL)(利达牌),一次性无菌纱布(德洁纱)。
1.3.2 抽滤系统折旧计算根据政府会计制度及《中华人民共和国企业所得税法实施条例》[11],采用平均年限法计算六联抽滤系统的年折旧额,年折旧额=固定资产原值/预计使用年限。本研究中使用的固定资产六联抽滤系统原价值9 840元,按此方法折算,每年成本为9 840/10=984元。
1.3.3 时间成本分别使用滤膜法和涂抹法接种30支内镜洗脱液,并统计总花费时间,分别计算出使用滤膜法和涂抹法接种每支内镜洗脱液平均花费时间。
1.4 统计分析应用SPSS20.0软件进行统计分析,非正态分布资料采用中位数(四分位数)描述,非正态分布两样本定量资料间比较采用Mann-Whitney U检验。计数资料两组比较采用χ2检验或Fisher精确概率法,用箱式图描述内镜菌落数数据的分散情况。P≤0.05为差异具有统计学意义。
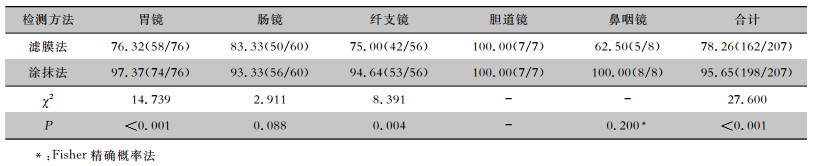
2 结果 2.1 滤膜法与涂抹法检测合格率的比较共检测软式内镜207支,其中胃镜76支、肠镜60支、纤支镜56支、胆道镜7支、鼻咽镜8支。滤膜法与涂抹法的检测合格率分别为78.26%、95.65%,差异有统计学意义(P<0.001)。采用滤膜法检测胃镜、纤支镜的清洗消毒合格率均低于涂抹法,差异有统计学意义(P<0.05)。见表 1。
| 表 1 滤膜法与涂抹法检测内镜清洗消毒合格率的比较(%) Table 1 Comparison in qualified rates of endoscope cleaning and disinfection detected with membrane filtration method and smear method(%) |
|
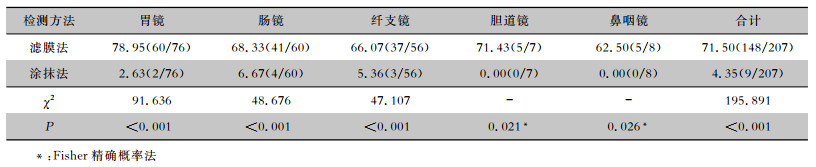
检测软式内镜清洗消毒效果,滤膜法病原菌检出率(71.50%)高于涂抹法病原菌检出率(4.35%),差异有统计学意义(P<0.001)。采用滤膜法检测的5类内镜清洗消毒后的病原菌检出率均高于涂抹法(P<0.05)。见表 2。
| 表 2 滤膜法与涂抹法检测清洗消毒后内镜病原菌检出率的比较(%) Table 2 Comparison in pathogen isolation rates of cleaned and disinfected endoscopes detected with membrane filtration method and smear method(%) |
|
内镜检出的菌落数滤膜法高于涂抹法,差异有统计学意义(P<0.001);胃镜、肠镜、纤支镜、胆道镜滤膜法检出菌落数均高于涂抹法,差异均有统计学意义(均P<0.05)。见表 3、图 2。
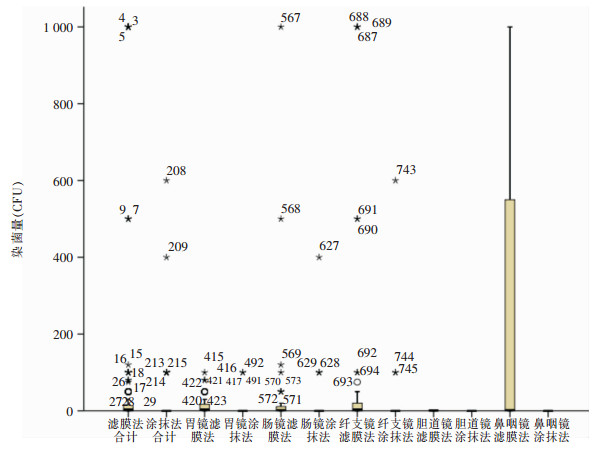 |
| 注:图中“*”及数值代表离群值观察单位的编号 图 2 不同检测方法检出清洗消毒后内镜菌落计数分布图 Figure 2 Distribution of bacterial colony counts of cleaned and disinfected endoscopes detected with different methods |
| 表 3 滤膜法与涂抹法检测清洗消毒后内镜菌落数的比较(CFU/件) Table 3 Comparison in bacterial colony counts of cleaned and disinfected endoscopes detected with membrane filtration method and smear method(CFU/piece) |

|
207支内镜滤膜法相较涂抹法每年增加经济成本1 498.48元,包括滤膜455.4元,一次性无菌纱布31.08元,75%乙醇消毒剂28元,6联抽滤系统984元。平均每支内镜滤膜法比涂抹法增加7.24元/次。使用滤膜法消耗的时间成本(124 s)高于涂抹法(62 s),使用滤膜法平均每支内镜多耗时62 s。
2.5 内镜消毒效果检测方法的问卷调查结果共收到来自江苏省、安徽省、重庆市及青海省4个省及省级行政区共14个城市的26所医院的调查反馈,包含三级甲等医院10所,三级乙等医院6所,二级甲等医院4所,二级乙等医院1所,其他医院5所。有2所医院使用滤膜法,使用涂抹法或倾注法的医院各11所,有1所医院使用倾注法结合ATP方法,1所医院使用涂抹法结合倾注法。如使用滤膜法检测内镜清洗消毒效果,医院最关注的问题为增加的经济成本(84.62%),其次为滤膜法与涂抹法的合格率区别(73.08%)、滤膜法的操作流程(73.08%)及增加的工作时间(69.23%)。
3 讨论内镜是精细、复杂而且需要复用的设备[12],在消化系统疾病的诊治中频繁被使用,有报道[13]显示,美国平均每年有2 000万例患者接受胃肠道内镜检查。2006年Nelson等[14]指出内镜检查治疗实际导致的感染要比报道的高很多。有报道[6, 15]称,近十五年来公开报道的内镜相关感染暴发事件有多起与逆行胰胆管造影术有关,均为内镜清洗消毒不彻底造成的。消毒效果检测是评价清洗消毒效果是否达标的重要方法。消毒效果检测可分为两类,一类是微生物培养;另一类是非微生物培养,包括蛋白残留测定、ATP生物荧光测定和PCR检测[16]。
已发布的大多数指南多以微生物培养作为检测方法[16]。根据中华人民共和国药典微生物限度检测[17],常用的细菌接种方法为倾注法、涂抹法及滤膜法。本研究结果显示,92.31%医院的内镜消毒效果检测方法为倾注法或涂抹法,仅有7.69%医院使用滤膜法。未使用滤膜法的医院主要顾虑为经济成本的消耗、滤膜法的检测效果、滤膜法的操作流程以及工作时间的消耗,其中最关注的为经济成本的消耗。分析原因为多数医院的常规检测方法以倾注法和涂抹法为主,如需更换为新的检测方法,无论是向医院申请还是自身操作的需求,都要考虑到成本(经济成本+时间成本)、效益(检测效果)及操作流程。
清洗消毒效果检测合格率是评价检测方法的“黄金”指标。更快速、准确的检测方法可以及时发现清洗消毒不合格的内镜,并进行原因分析及整改,使常规监测更具意义。本研究中滤膜法检测合格率低于涂抹法(78.26% VS 95.65%),滤膜法可以多检出17.39%的清洗消毒不合格内镜。涂抹法相对滤膜法会导致一部分清洗消毒不合格的内镜被判定为清洗消毒合格,存在可能导致患者交叉感染甚至感染暴发的风险。本研究中滤膜法检测内镜合格率(78.26%)与朱艳秋等[18]研究中滤膜法合格率(88.60%)及Chiu等[19]研究中滤膜法合格率(89.3%)有一定差距,考虑原因为2018年初该院启用新大楼及新内镜中心,验收过程中的模拟检测结果也纳入了本研究。虽然大部分的涂抹法检测结果为无菌生长,这并不一定意味着该内镜通道是无菌的,实际上,内镜采样容易出现假阴性结果[20]。本研究中,滤膜法检测内镜病原菌检出率及菌落数高于涂抹法,表明相对于涂抹法,滤膜法可以更有效的培养出内镜洗脱液中的细菌,更精确、客观的反映内镜的清洗消毒效果。本研究共检测207支内镜,滤膜法比涂抹法经济成本增加1 498.48元/年,每支内镜使用滤膜法检测仅比使用涂抹法多花费经济成本降低了7.24元/次,而却能多检出17.39%的不合格内镜,降低了内镜相关感染发生的风险。内镜相关的最新感染事件在2017年7月,弗吉尼亚梅森医院内十二指肠镜超级细菌感染的暴发,梅森医院赔偿一例死亡患者家属100万美元。对比一旦发生感染暴发对患者及医院造成的损失,滤膜法的经济成本投入是极其必要且有价值的。另外,在时间成本上,每检测一支内镜滤膜法比涂抹法仅多花费62 s,分析原因主要因为滤膜法的步骤相对较多,且为保证结果可靠,在使用滤膜法进行不同批次内镜洗脱液接种之间,需要对相关物品进行消毒干燥。所以滤膜法相对涂抹法,会增加接种人员的工作量。
内镜在消化系统诊治中频繁使用,已然成为消化内科医生的“第三只眼睛”,为了确保患者的安全,医疗机构应严格按规范执行内镜清洗消毒程序,并做好消化内镜消毒效果监测。建议各级医疗机构,在条件允许的情况下,积极使用滤膜法进行内镜的清洗消毒监测,及时发现内镜消毒工作中存在的问题并持续质量改进,提高清洗消毒质量,保障患者医疗安全。
致谢: 谨对参与调查的26所医院表示衷心的感谢!
| [1] |
宁培勇, 纪学悦, 丁津华, 等.不同检测方法对内镜消毒效果监测的应用性研究[J/OL].中国内镜杂.http://kns.cnki.net/kcms/detail/43.1256.R.20190308.1044.002.html.
|
| [2] |
Kovaleva J, Meesen N E, Peters FT, et al. Is bacteriologic surveillance in endoscope reprocessing stringent enough?[J]. Endoscopy, 2009, 41(10): 913-916. DOI:10.1055/s-0029-1215086 |
| [3] |
FrǎtilǎO, Tantǎu M. Cleaning and disinfection in gastrointestinal endoscopy:current status in Romania[J]. J Gastrointestin Liver Dis, 2006, 15(1): 89-93. |
| [4] |
Noronha AM, Brozak S. A 21st century nosocomial issue with endoscopes[J]. BMJ, 2014, 348: g2047. DOI:10.1136/bmj.g2047 |
| [5] |
蔡玲, 张浩军, 杨亚红. 内镜相关感染及其预防与控制研究进展[J]. 中国感染控制杂志, 2016, 15(7): 533-536. DOI:10.3969/j.issn.1671-9638.2016.07.025 |
| [6] |
Muscarella LF. Risk of transmission of carbapenem-resistant Enterobacteriaceae and related "superbugs" during gastrointestinal endoscopy[J]. World J Gastrointest Endosc, 2014, 6(10): 457-474. DOI:10.4253/wjge.v6.i10.457 |
| [7] |
Bajolet O, Ciocan D, Vallet C, et al. Gastroscopy-associated transmission of extended-spectrum beta-lactamase-producing Pseudomonas aeruginosa[J]. J Hosp Infect, 2013, 83(4): 341-343. DOI:10.1016/j.jhin.2012.10.016 |
| [8] |
纪学悦, 费春楠, 刘军, 等. 天津市消化内镜使用情况调查及消毒灭菌的影响因素分析[J]. 中华医院感染学杂志, 2017, 27(14): 3354-3357. |
| [9] |
中华人民共和国国家卫生和计划生育委员会.软式内镜清洗消毒技术规范: WS 507-2016[S].北京, 2016.
|
| [10] |
中华人民共和国卫生部.医院消毒卫生标准: GB 15982-2012[S].北京, 2012.
|
| [11] |
中华人民共和国国务院.中华人民共和国企业所得税法实施条例[EB/OL].(2007-12-11)[2019-04-01].http://www.gov.cn/zwgk/2007-12/11/content_830645.htm.
|
| [12] |
Kenters N, Huijskens EG, Meier C, et al. Infectious diseases linked to cross-contamination of flexible endoscopes[J]. Endosc Int Open, 2015, 3(4): E259-E265. DOI:10.1055/s-00025476 |
| [13] |
Petersen BT, Chennat J, Cohen J, et al. Multisociety guideline on reprocessing flexible gastrointestinal endoscopes:2011[J]. Gastrointest Endosc, 2011, 73(6): 1075-1084. DOI:10.1016/j.gie.2011.03.1183 |
| [14] |
Nelson DB, Muscarella LF. Current issues in endoscope reprocessing and infection control during gastrointestinal endoscopy[J]. World J Gastroenterol, 2006, 12(25): 3953-3964. DOI:10.3748/wjg.v12.i25.3953 |
| [15] |
Ryu JK, Kim EY, Kwon KA, et al. Role of clinical endoscopy in emphasizing endoscope disinfection[J]. Clin Endosc, 2015, 48(5): 351-355. DOI:10.5946/ce.2015.48.5.351 |
| [16] |
Shin SP, Kim WH. Recent update on microbiological monitoring of gastrointestinal endoscopes after high-level disinfection[J]. Clin Endosc, 2015, 48(5): 369-373. DOI:10.5946/ce.2015.48.5.369 |
| [17] |
国家药典委员会. 中华人民共和国药典[M]. 北京: 中国医药科技出版社, 2015.
|
| [18] |
朱艳秋, 张满, 杨怀, 等. 滤膜法与倾注法两种方法检测内镜消毒效果的结果比较[J]. 中国感染控制杂志, 2018, 17(6): 539-542. DOI:10.3969/j.issn.1671-9638.2018.06.016 |
| [19] |
Chiu KW, Tsai MC, Wu KL, et al. Surveillance cultures of samples obtained from biopsy channels and automated endoscope reprocessors after high-level disinfection of gastrointestinal endoscopes[J]. BMC Gastroenterol, 2012, 12: 120. DOI:10.1186/1471-230X-12-120 |
| [20] |
Muscarella LF: The study of a contaminated colonoscope[J].Clin Gastroenterol Hepatol, 2010, 8: 577-580.
|



