颅内感染是开放性颅脑外伤及开颅手术的常见并发症之一。脑脊液阳性致病菌检出率低等原因[1], 目前抗感染治疗仍以经验治疗为主。血-脑屏障的存在, 使得很多抗菌药物难以进入脑脊液循环, 敏感药物透过率低, 更增加了抗感染治疗的难度。近年来多重耐药(multi-drug resistance, MDR)或泛耐药(extensive drug resistance, XDR)鲍曼不动杆菌颅内感染病例报道不断增加, 此类高病残率/病死率的难治性颅内感染已经给神经外科抗感染治疗带来了严峻挑战。本文报告1例经鼻视神经管减压术后XDR鲍曼不动杆菌颅内感染病例的诊治经历, 并回顾分析近5年相关文献。
1 病历资料 1.1 病史患者男性, 56岁, 2017年2月5日以"坠落伤"于本院就诊。患者伤后神志清, GCS评分15分。左眼视力丧失, 直接光反应阴性, 间接光反应阳性, 右眼正常, 伴脑脊液鼻漏。颅脑CT显示:左侧额叶脑挫裂伤, 多发颅底骨折, 左侧视神经管骨折。
1.2 诊疗及转归伤后50 h接受经鼻行视神经减压手术, 术中可见后组筛窦、蝶窦骨折较重, 左侧视神经管开放性骨折, 内侧壁及下壁近眶口处骨折片内陷压迫视神经(见图 1-c)。术中视神经管全程骨性开放并松解视神经鞘膜(见图 1-d)。术后给予静脉滴注头孢曲松钠(2.0 g, q12h), 甲强龙500 mg/d连用3 d冲击治疗, 以及神经营养等药物治疗。术后患者无发热, 自觉脑脊液鼻漏减轻, 术后第4天患者左眼光感恢复。术后第5天突发抽搐, 伴高热(38℃~39℃)、昏迷。血常规:白细胞计数(WBC) 14.68×109/L, 中性粒细胞百分比(NE%)93.9%, 降钙素原(PCT)14.47 ng/mL, 更换抗生素为万古霉素(1.0 g, q12h)联合美罗培南(1.0 g, q8h)静脉滴注抗感染治疗。次日, 患者生命体征平稳后给予腰穿并置管引流, 可见脑脊液黄色、浑浊、米浆样(图 1-f), 压力高, 送脑脊液进行常规检查及培养, 细胞数10 228×106/L, 总蛋白>3 000 mg/L, 葡萄糖<1.1 mmol/L; 涂片找到G-杆菌, 确诊为颅内感染, 等待药敏结果, 并维持原方案抗感染。术后第7天患者病情加重, 高热昏迷, 痰量多, 排痰困难, 高流量吸氧(4~6 L/min)下血氧饱和度仅90%, 气管切开后转入神经外科重症监护室(neurosurgery inten- sive care unit, NICU), 呼吸机压力支持通气模式辅助通气。再次送脑脊液进行常规检查及培养, 细胞数10 115×106/L。连续两次脑脊液培养药敏结果均显示为XDR鲍曼不动杆菌, 仅对替加环素及复方磺胺甲
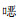
 |
| a:术前影像学检查; b:术后影像学检查; c:减压前内镜下视神经管; d:减压后视神经; e:2月11日颅脑磁共振弥散影像; f:历次脑脊液标本; WBC为历次脑脊液常规细胞数(×106/L) 图 1 XDR鲍曼不动杆菌颅内感染病例治疗方案及效果图 Figure 1 Treatment plan and efficacy of XDR Acinetobacter baumannii intracranial infection |
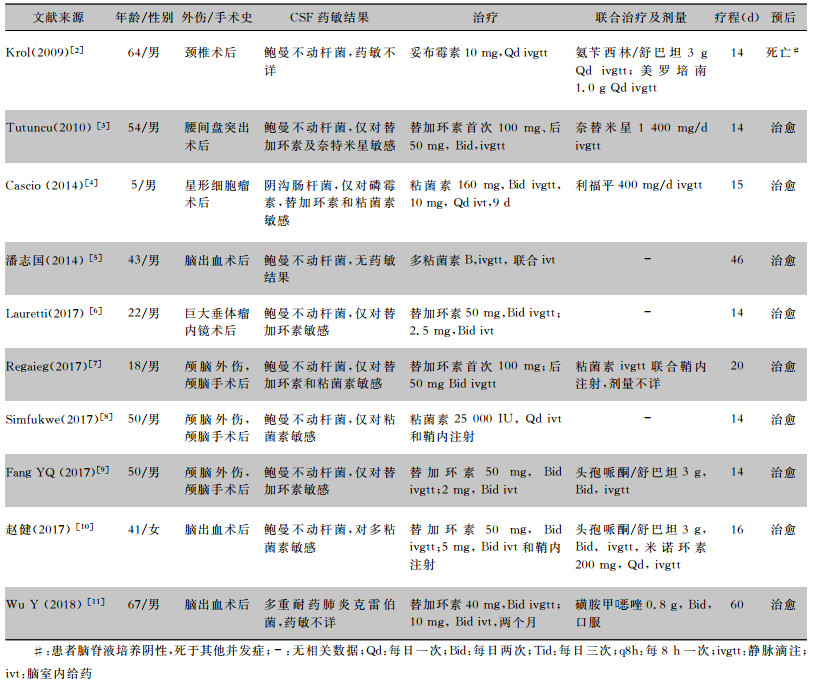
| 表 1 2009-2018年颅内鲍曼不动杆菌感染鞘内注射相关文献 Table 1 Literatures on intrathecal injection for treatment of Acinetobacter baumannii infection from 2009 to 2018 |
|
鲍曼不动杆菌为条件致病菌, 广泛分布于人体呼吸道中, 正常生理条件下不会引起重症感染[12]。具有NICU停留史的患者多发生MDR、甚至XDR鲍曼不动杆菌感染[13], 此类鲍曼不动杆菌是引发难治性颅内感染的元凶。中枢神经系统感染多与颅脑外伤或颅脑手术有关[2]。此外, 急性生理应激和严重创伤、脑脊液漏、大剂量糖皮质激素及广谱抗菌药物的使用等也是颅内感染的高危因素[14]。本例患者开放性颅脑外伤后脑脊液鼻漏破坏了正常的血脑屏障, 并接受经鼻内镜行视神经减压手术治疗, 且术后还应用了糖皮质激素冲击疗法, 以上多种危险因素最终导致患者发生XDR鲍曼不动杆菌颅内感染。
颅内感染脑脊液的病原菌检出率很低[1], 颅脑手术后颅内鲍曼不动杆菌感染的发生率为2.00% ~27.59%[15], 且常发生于手术后3~7 d。鲍曼不动杆菌引起的中枢系统感染占医院脑膜炎的3.6% ~11.2%[16], 由MDR或XDR菌株引起的感染预后极差, 病死率高达72.7%[17], 幸运的是此次患者感染的鲍曼不动杆菌是XDR而非全耐药, 以往作为抗鲍曼不动杆菌感染的首选药物碳青霉烯类抗生素[18]在本病例感染菌株多次药敏结果中均提示耐药, 因而选用替加环素单一静脉给药3 d, 感染未见控制。考虑到替加环素的血脑屏障透过率仅为11%[19], 经家属知情同意后增加鞘内给药。综合以往文献报道, 最终采取2.5 mg配伍5 mL生理盐水, 每日两次鞘内给药后夹闭引流管2 h的方案。另外文献报道舒巴坦对抗鲍曼不动杆菌有效[20], 临床上无法取得舒巴坦单剂, 因此选用头孢哌酮钠舒巴坦钠作为第三联药物, 并且使用极量, 以最大程度利用其中的舒巴坦成分。在目标治疗的基础上, 保持腰大池引流的通畅也是抗感染成功的关键, 鲍曼不动杆菌的脑脊液蛋白成分极高, 极易堵管, 若发生堵管应及时更换新引流管。通畅的脑脊液引流配合合理的敏感抗菌药物治疗是神经外科抗耐药杆菌感染治疗成功的关键, 与相关文献[21]报道一致。
目前, 对不动杆菌属敏感性较好的抗生素主要是多黏菌素和替加环素[22]。但多黏菌素在国内使用较少, 本院无法获得, 因此选用药敏结果中敏感药物替加环素。替加环素是一种抗菌谱可以覆盖革兰阴性杆菌及革兰阳性球菌的甘氨酰环素类广谱抗菌药物[23], 对泛耐药病原菌有较好活性, 临床上应用逐渐增多。替加环素在国内外上市时间较短, 缺乏大样本量病例研究。近年, 有静脉滴注替加环素发生凝血功能障碍、弥散性血管内凝血及急性胰腺炎等药物不良反应的相关报道[24]。目前, 在为数尚不多的联合脑室内或腰大池鞘内注射替加环素成功治疗鲍曼不动杆菌颅内感染的文献中, 在治疗过程中均未出现药物毒副作用[6, 9-10]。本病例鞘内注射替加环素也未发现神经毒性副作用, 尽管如此, 依然要警惕鞘内注射抗菌药物易出现的如头痛、下肢麻木、肛门坠胀感以及癫痫等不良反应, 必要时采用微量泵控制鞘内给药速度[25]。目前的临床指南[9]和替加环素药品说明书[23]均未曾提及鞘内注射使用方式, 因此呼吁最新的抗感染临床指南应根据临床需要进行相应修改。
综上所述, 鞘内注射替加环素可能是重症MDR或XDR鲍曼不动杆菌颅内感染患者的有效治疗选择。然而, 因现有有效病例尚少, 无法准确预测鞘内注射替加环素的毒副作用。需更多的研究进一步证明鞘内注射替加环素对颅内感染的治疗价值, 且不仅仅局限于鲍曼不动杆菌感染。虽然该病例仅是个案报告, 但本病例的治疗方案、剂量及给药频率能够为耐药性鲍曼不动杆菌颅内感染治疗提供有利的临床证据, 具有一定的借鉴意义。
| [1] |
Gaynes R, Edwards JR. Overview of nosocomial infections caused by gram-negative bacilli[J]. Clin Infect Dis, 2005, 41(6): 848-854. DOI:10.1086/432803 |
| [2] |
Krol V, Hamid NS, Cunha BA. Neurosurgically related nosocomial Acinetobacter baumannii meningitis:report of two cases and literature review[J]. J Hosp Infect, 2009, 71(2): 176-180. DOI:10.1016/j.jhin.2008.09.018 |
| [3] |
Tutuncu EE, Kuscu F, Gurbuz Y, et al. Tigecycline use in two cases with multidrug-resistant Acinetobacter baumannii meningitis[J]. Int J Infect Dis, 2010, 14(Suppl 3): e224-e226. |
| [4] |
Cascio A, Mezzatesta ML, Odierna A, et al. Extended-spectrum beta-lactamase-producing and carbapenemase-producing Enterobacter cloacae ventriculitis successfully treated with intraventricular colistin[J]. Int J Infect Dis, 2014, 20: 66-67. DOI:10.1016/j.ijid.2013.11.012 |
| [5] |
潘志国, 苏磊. 成功救治泛耐药鲍曼不动杆菌致颅内感染1例[J]. 感染、炎症、修复, 2014, 15(1): 54-55. DOI:10.3969/j.issn.1672-8521.2014.01.018 |
| [6] |
Lauretti L, D'Alessandris QG, Fantoni M, et al. First reported case of intraventricular tigecycline for meningitis from extremely drug-resistant Acinetobacter baumannii[J]. J Neurosurg, 2017, 127(2): 370-373. DOI:10.3171/2016.6.JNS16352 |
| [7] |
Regaieg K, Bahloul M, Turki O, et al. The efficacy of the tigecycline-colistin association in the treatment of multi-resis-tant Acinetobacter baumannii meningitis[J]. Med Mal Infect, 2017, 47(2): 175-177. DOI:10.1016/j.medmal.2017.01.003 |
| [8] |
Simfukwe K, Zhou Y, Han G, et al. Management of intracranial ventriculitis caused by multidrug resistant Acinetobacter baumannii:case report and literature review[J]. Med J Zam-bia, 2017, 44(1): 58-63. |
| [9] |
Fang YQ, Zhan RC, Jia W, et al. A case report of intraven-tricular tigecycline therapy for intracranial infection with extremely drug resistant Acinetobacter baumannii[J]. Medicine (Baltimore), 2017, 96(31): e7703. DOI:10.1097/MD.0000000000007703 |
| [10] |
赵健, 王仙, 张双, 等. 开颅术后并发泛耐药鲍曼不动杆菌性颅内感染病例报告并文献复习[J]. 临床神经外科杂志, 2017, 14(4): 310-312. DOI:10.3969/j.issn.1672-7770.2017.04.018 |
| [11] |
Wu Y, Chen K, Zhao J, et al. Intraventricular administration of tigecycline for the treatment of multidrug-resistant bacterial meningitis after craniotomy:a case report[J]. J Chemother, 2018, 30(1): 49-52. DOI:10.1080/1120009X.2017.1338846 |
| [12] |
缪应纯, 徐晓林, 缪应举, 等. 鲍曼不动杆菌研究进展[J]. 山东化工, 2017, 46(23): 49-51. DOI:10.3969/j.issn.1008-021X.2017.23.022 |
| [13] |
Brigante G, Migliavacca R, Bramati S, et al. Emergence and spread of a multidrug-resistant Acinetobacter baumannii clone producing both the carbapenemase OXA-23 and the 16S rRNA methylase ArmA[J]. J Med Microbiol, 2012, 61(Pt 5): 653-661. |
| [14] |
Pogue JM, Mann T, Barber KE, et al. Carbapenem-resistant Acinetobacter baumannii:epidemiology, surveillance and management[J]. Expert Rev Anti Infect Ther, 2013, 11(4): 383-393. DOI:10.1586/eri.13.14 |
| [15] |
Tafelski S, Wagner L, Angermair S, et al. Therapeutic drug monitoring for colistin therapy in severe multi-resistant Acinetobacter intracerebral abscess:A single case study with high-dose colistin and review of literature[J]. SAGE Open Med Case Rep, 2017, 5: 2050313X17711630. |
| [16] |
Yiş R. Evaluation of blood cultures in a children's hospital located in Southeastern Anatolia[J]. Turk Pediatri Ars, 2015, 50(2): 102-107. DOI:10.5152/TurkPediatriArs. |
| [17] |
Jawad A, Seifert H, Snelling AM, et al. Survival of Acinetobacter baumannii on dry surfaces:comparison of outbreak and sporadic isolates[J]. J Clin Microbiol, 1998, 36(7): 1938-1941. |
| [18] |
陈佰义, 何礼贤, 胡必杰. 中国鲍曼不动杆菌感染诊治与防控专家共识[J]. 中华医学杂志, 2012, 92(2): 76-85. DOI:10.3760/cma.j.issn.0376-2491.2012.02.002 |
| [19] |
Rodvold KA, Gotfried MH, Cwik M, et al. Serum, tissue and body fluid concentrations of tigecycline after a single 100 mg dose[J]. J Antimicrob Chemother, 2006, 58(6): 1221-1229. DOI:10.1093/jac/dkl403 |
| [20] |
黎金海, 陈嘉伟, 郭旭光. 替加环素联合舒巴坦对泛耐药鲍曼不动杆菌体外抗菌活性研究[J]. 今日药学, 2016, 26(7): 482-488. |
| [21] |
苏小妹, 邱前辉, 詹建东, 等. 鼻内镜下视神经减压术治疗外伤性视神经损伤临床观察[J]. 中国耳鼻咽喉颅底外科杂志, 2017, 23(4): 323-327. |
| [22] |
Cunha BA. Pharmacokinetic considerations regarding tigecycline for multidrug-resistant (MDR) Klebsiella pneumoniae or MDR Acinetobacter baumannii urosepsis[J]. J Clin Microbiol, 2009, 47(5): 1613. DOI:10.1128/JCM.00404-09 |
| [23] |
Pankey GA. Tigecycline[J]. J Antimicrob Chemother, 2005, 56(3): 470-480. DOI:10.1093/jac/dki248 |
| [24] |
刘峰, 邓贵新, 刘锐锋. 21例替加环素致药品不良反应[J]. 中国医院用药评价与分析, 2018, 18(7): 1000-1004. |
| [25] |
严建泉, 钱东翔, 罗鹏, 等. 万古霉素微量泵控制持续鞘内注射治疗颅内感染[J]. 实用临床医药杂志, 2014, 18(7): 91-93. |



